Antiviraalisten aineiden kliininen farmakologia. Antiviraaliset aineet. Luokitus. Toimintamekanismit. Sovellus. Sivuvaikutukset
Antiviraaliset lääkkeet ovat lääkkeitä, jotka on tarkoitettu erilaisten virussairauksien hoitoon: influenssa, herpes, HIV -infektio jne. Niitä käytetään myös ennaltaehkäiseviin tarkoituksiin. Bakteereja ja viruksia, jotka voivat aiheuttaa vilustumista (akuutteja hengitystieinfektioita), on jatkuvasti mukana ympäristöön... Ensimmäinen spesifiseksi viruslääkkeeksi ehdotettu lääke oli K -tiosemikarbatsoni. Antiviraaliset lääkkeet on tarkoitettu erilaisten virussairauksien (influenssa, herpes, HIV -infektio jne.) Hoitoon. On paljon vähemmän kliinisesti osoittautuneita viruslääkkeitä kuin antibiootteja. Samaan aikaan ensimmäiset viruslääkkeet saatiin vasta 1970 -luvun lopulla. Erityisiä viruslääkkeitä ei ole kehitetty tarttuvan mononukleoosin (EBV -infektio) hoitoon. Onko olemassa laajakirjoisia viruslääkkeitä kaikkiin influenssaviruksiin? Mitä voit antaa lapsille? Antiviraaliset lääkkeet: arbidoli, anaferoni, oscillococcinum jne. Influenssaa käytettäessä käytetään etiotrooppisten, patogeenisten ja oireenmukaisten aineiden kompleksia, taudin aiheuttajaa, viruksenvastaista lääkettä, kehon vieroitusta, lisääntynyttä puolustuskykyä, tulehduksellisten ja muiden muutosten poistamista. Lievien ja kohtalaisten influenssamuotojen hoito suoritetaan kotona, vaikea ja monimutkainen - tartuntatautien sairaalassa. ARVI: n monimutkaisessa hoidossa on käytettävä lääkkeitä, joilla on suora antiviraalinen vaikutus ja joilla on laaja vaikutus hengityselinten viruksia vastaan. ARVI: n ja influenssan hoidossa käytettävien lääkkeiden valikoima on laaja ja monipuolinen. Venäjällä käytetään alkuperäisiä viruslääkkeitä, jotka on luotu kotimaisen kehityksen perusteella. Antiviraalinen lääke remantadiini tehokas hoidettaessa tyypin A viruksen aiheuttamaa influenssaa ja vain sen varhaisessa käytössä - ensimmäisinä tunteina ja päivinä taudin alkamisesta (0,1 g 3 kertaa päivässä aterioiden jälkeen ensimmäisenä päivänä, 0,1 g 2 kertaa päivässä 2. ja 3. päivänä ja 0,1 g kerran 4. sairauspäivänä). Tyypin A ja B virusten aiheuttaman influenssan hoitoon lääke on tehokas oseltamiviiri(Tamiflu) aikuisille ja yli 12 -vuotiaille lapsille, 0,075 g 2 kertaa päivässä 5 päivän ajan. Tehokas on lääkkeiden käyttö, jotka stimuloivat omien endogeenisten interferonien tuotantoa, ts. interferonia indusoivat ja immunomoduloivat lääkkeet (arbidoli, amiksiini, neoviiri, sykloferoni). Antiviraalinen lääke Arbidol tehokas influenssa A- ja B -viruksia ja muiden akuuttien hengitystieinfektioiden patogeenejä vastaan. Se on määrätty aikuisille ja yli 12 -vuotiaille lapsille, 0,2 g 3-4 kertaa päivässä ennen ateriaa 3-5 päivän ajan. WHO ei pidä arbidolia tai muita kemiallisesti samankaltaisia aineita lupaavina viruslääkkeinä. Lääke kuuluu vähätoksisiin lääkkeisiin (keskimääräinen tappava annos on yli 4 g / kg). Amiksin - tehokas sekä influenssaviruksia että kaikkien akuuttien hengitystieinfektioiden patogeeneja vastaan. Terapeuttiset annokset aikuisille ovat 0,125 g kerran päivässä suun kautta aterian jälkeen 2 peräkkäisen päivän ajan, sitten 0,125 g joka toinen päivä (mutta enintään 6 tablettia hoitojaksoa kohden). Neovir Sitä käytetään parainfluenssavirusten, rinovirusten, RS -viruksen, adenovirusten ja herpesvirusten aiheuttamien influenssan ja ARVI: n hoitoon. Terapeuttisia tarkoituksia varten suositellaan yhdestä 2 ml: n 12,5% liuoksen lihaksensisäisestä injektiosta neljään injektioon 48 tunnin välein (kurssin vakavuudesta riippuen). Cycloferon - endogeenisen interferonin indusoija, jolla on voimakas antiviraalinen, immunomoduloiva ja anti-inflammatorinen vaikutus. Komplisoitumattoman influenssan terapeuttiset annokset: 1. päivänä 4 tablettia kerrallaan, 2., 4. ja 6. päivänä 2 tablettia (0,15 g) kerran päivässä ennen ateriaa. Cycloferon 5% linimenttiä käytetään ulkoiseen intranasaaliseen käyttöön. Kun influenssa esiintyy lievässä ja keskivaikeassa mutkattomassa muodossa, käytetään alfa -interferonivalmisteita - ihmisen leukosyyttien interferonia (HRI), jolla on alhainen viruslääke. Se tiputetaan nenän kautta, 5 tippaa vähintään 5-6 kertaa päivässä tai annetaan inhalaationa 2 kertaa päivässä (2-3 päivän kuluessa), kun ensimmäinen ilmestyy. kliiniset oireet flunssa ja muut akuutit hengitystieinfektiot. PMI: tä, jolla on korkea antiviraalinen aktiivisuus, käytetään injektioissa aikuisten vakavan ja monimutkaisen flunssan ja muiden akuuttien hengitystieinfektioiden hoitoon. Keuhkoputkien tyhjennystoiminnon parantamiseksi ja liman ja ysköksen evakuoinnin parantamiseksi on tarpeen suorittaa lämpimiä, märkiä inhalaatioita, jotka sisältävät soodaa ja keuhkoputkia laajentavia aineita (solutani, aminofylliini, efedriini). Hengitys suoritetaan enintään 15 minuuttia 2 kertaa päivässä 4 päivän ajan. Vaikeassa nuhassa 2–5% liuosta käytetään nenänsisäiseen antamiseen. efedriini, 0,1% liuos (tai emulsio) sanorina, naftizin, galazolin. Antibioottien tai sulfonamidien määrääminen komplikaatioiden (keuhkokuumeen) estämiseksi potilailla, joilla on mutkaton influenssa perusteeton, koska se usein edistää näiden komplikaatioiden kehittymistä. Vaikeaa influenssamuotoa sairastavien potilaiden monimutkainen hoito patogeenisten ja oireiden lisäksi sisältää erityisen etiotrooppisen hoidon. Tehokkain on influenssan vastaisen immunoglobuliinin(gamma -globuliini) injektoituna varhaiset päivämäärät sairaudet, 3–6 ml lihakseen 8–12 tunnin välein (lapsille - 0,15–0,2 ml / 1 kg painokiloa kohti päivässä), kunnes saavutetaan voimakas terapeuttinen vaikutus. Auttaako nämä lääkkeet adenovirusinfektioon? Potilaat, joilla on lievä ja keskivaikea komplikaatioton adenovirusinfektio, suoritetaan, kuten influenssan tapauksessa, patogeeninen ja oireenmukainen hoito poliklinikassa (kotona), sotilashenkilöstö - lääketieteellisen keskuksen eristysosastolla. Potilaita, joilla on vakavia ja monimutkaisia muotoja, hoidetaan tartuntatautien sairaaloissa. Näiden potilaiden monimutkainen hoito sisältää injektio lihakseen 6 ml normaalia immunoglobuliinia, joka sisältää spesifisiä vasta-aineita adenoviruksia vastaan, sekä detoksifikaatioliuosten (5% glukoosiliuos 500 ml, askorbiinihappo, hemodez 200-300 ml) laskimonsisäinen antaminen, vitamiinikompleksi, kostutettu happi nenän katetrien kautta. Antiviraalinen tee on hyödyllinen adenovirusinfektiossa. Se lievittää vatsakipua, joka liittyy tähän kylmään infektioon. Silmävaurion sattuessa immunoglobuliini tiputetaan sidekalvopussiin. Jos kyseessä on kalvoinen sidekalvotulehdus, silmät pestään 2% boorihapon liuoksella, 20-30% natriumsulfasyyliliuoksella (albusidi), 0,2% deoksiribonukleaasiliuoksella (tislatussa vedessä), 0,25-0,5% tebrofeenia voide asetetaan silmäluomien reunoille ... Kun kehittyy akuutti kurkunpään tracheobronkiitti ja kurkunpään ahtauma (väärä lantio), määrätään lihaksensisäinen lyyttinen seos (2,5% klooripromatsiiniliuos yhdessä 1% difenhydramiiniliuoksen ja 0,5% novokaiiniliuoksen kanssa - kaikki ikäannoksina). Sisällä - prednisoloni, alkaen 15-20 mg, annosta nostetaan asteittain. Hormonihoidon kesto on 5-7 päivää. Keuhkokuumeessa adenovirusinfektion monimutkaista hoitoa tehostetaan nimittämällä antibiootteja. Koska keuhkokuume on stafylokokki, oksasilliini, metisilliini esitetään tavanomaisissa ikäannoksissa 7-14 päivän ajan. Herpesinfektiopotilaiden hoidon perustana ovat etiotrooppiset toimenpiteet, jotka suoritetaan solunsalpaajalääkkeen asykloviirin (synonyymit - virolex, zovirax), interferonin ja interferonogeenien - amiksiinin avulla. Niiden tehokkuus on paljon parempi, kun hoito aloitetaan varhain ( sairauden ensimmäisinä päivinä). Ihon ja limakalvojen herpeettisten vaurioiden tapauksessa, mukaan lukien - sukupuolielinten herpes, 200 mg asykloviiria määrätään 5 kertaa päivässä 7-10 päivän ajan tai amixin 0,125 g kerran päivässä 1, 2, 4, 6, 8, 10, 12, 14, 16 ja 18 päivää (10 tablettia hoitojaksoa kohden). Jos sinulla on sairaus, johon liittyy yksittäisiä pieniä ihottumia iholla tai huulilla, voit rajoittua amiksiinin ottamiseen ja Zoviraxin 5% voiteen (voiteen) paikalliseen käyttöön. Herpeettiseen proktiittiin tulee määrätä 400 mg asykloviiria Yleistyneille ja viskeraalisille herpesinfektion muodoille suositellaan laskimonsisäistä asykloviiriliuoksen antamista 15-30 mg / kg vuorokaudessa (vuorokausiannos annetaan 3 annoksena - 8 tunnin kuluttua) vähintään 10 päivän ajan ja interferonivalmisteet (Reaferon, 1-3 miljoonaa .U / vrk tai muut). Sarveiskalvon herpeettisten vaurioiden tapauksessa on käytettävä paikallisia interferonin, vidorabiinin ja asykloviirin liuoksia. Etiotrooppisen hoidon ohella suoritetaan patogeenisiä (taudin kliinistä muotoa vastaavia) toimenpiteitä. Ennuste. Yleistynyt herpesinfektio sekä aivotulehdus, hepatiitti, keuhkokuume, ilman etiotrooppista hoitoa, päättyy kuolemaan 60-90%: ssa tapauksista. Silmän herpeettiset vauriot voivat aiheuttaa näön menetyksen. Ihon ja limakalvojen herpesinfektio HIV-tartunnan saaneilla potilailla voi olla monimutkainen syvällä haavaumaprosessilla, jolla on taipumus krooniseen kulkuun.Antiviraaliset lääkkeet ARVI: n hoidossa
LÄÄKEVALMISTEET ADENOVIRAL INFECTION
ANTIVIRAALISET LÄÄKKEET HERPEETTISIIN TUOTTEISIIN
5 kertaa päivässä 8-12 päivän ajan ja amiksiini 0,125 g - 1 kerta päivässä hoitopäivinä 1, 2, 4, 6, 8, 10, 12, 14, 16 ja 18 (10 tablettia hoitojaksoa kohden).
UKRAINAN KOULUTUS- JA TIETEET
UKRAINAN VALTION KEMIALLIS-TEKNOLOGINEN YLIOPISTO
HTOV -osasto
KURSSITYÖ
"ANTIVIRAALISET LÄÄKKEET"
Dnepropetrovsk 2005
JOHDANTO
1. YLEISET MÄÄRÄYKSET
2. VIRUSTUSVÄLINEIDEN LUOMISHISTORIA
3. Antiviraalisten aineiden luokittelu
A) Interferoni
Interferonin induktorit
B) Amantadiinin ja muiden synteettisten yhdisteiden ryhmien johdannaiset
C) Nukleosidit
D) Kasviperäiset viruslääkkeet
4. BIOLOGISEN TOIMINNAN MEKANISMI
4.1. Influenssan vastaiset lääkkeet
4.2. Antiherpeettiset ja sytomegaloviruslääkkeet
4.3. Ihmisen immuunikatovirukseen (HIV) vaikuttavat lääkkeet (tsidovutsiini, fosfonoformaatti)
4.5. Amiksin - mahdollisuudet ja näkymät soveltamiseen kliinisessä käytännössä
4.5.1. Amiksin -lääkkeen nimi ja kuvaus
4.5.2. Antiviraalinen aktiivisuus ja interferonia tuottavien solujen induktio.
4.5.3. Vaikutukset immuunijärjestelmään ja tulehdukseen.
4.5.4. Farmakokinetiikka
4.5.5. Prekliiniset tutkimukset lääkkeen antiviraalisesta aktiivisuudesta
5.1. Uudet reitit tiloronihydrokloridin synteesille
5.2. Bonaftonin saaminen (6-bromi-1,2-naftokinoni)
5.3. GOSSIPOL
5.4. LEUKOCYTE ALPHA INTERFERONIN HANKINTA
7. TAULUKKO viruslääkkeistä
KIRJALLISUUS
EHDOT -SANASTO
JOHDANTO
Virukset ovat ei-solullisia elämänmuotoja, joilla on oma perimänsä ja jotka kykenevät lisääntymään vain kehittyneempien olentojen soluissa. Viruksille on ominaista kaksi olemassaolon muotoa: solunulkoinen ja solunsisäinen (lisääntyvä). Virukset koostuvat kahdesta suuresta ryhmästä: yksinkertaisista ja monimutkaisista. Edelliset koostuvat vain proteiineista ja nukleiinihapoista, kun taas kompleksiset virukset sisältävät näiden komponenttien lisäksi lipidejä ja hiilihydraatteja glykoproteiinien muodossa. Viruksille on ominaista laaja valikoima nukleiinihappomuotoja, mukaan lukien ne RNA- ja DNA -muodot, joita ei ole solujen elämänmuodoissa.
Virusten lisääntyminen tapahtuu solussa. Monet virukset imeytyvät soluun pinosytoosin kautta. Häkkiin päästyään ne vapautuvat kuoresta. Virusten kehittymisen ensimmäiset vaiheet solussa koostuvat yleensä ns. Varhaisten proteiinien, ts. proteiinit ovat entsyymejä, joita virus tarvitsee replikoida nukleiinihappojaan. Niin kutsutut myöhäiset proteiinit osallistuvat tytärvirospoorien proteiinikalvojen muodostumiseen. DNA: ta sisältävien virusten entsyymeistä yksi ensimmäisistä on syntetisoitu RNA -polymeraasi, joka rakentaa informatiivisen RNA: n DNA -juosteeseen. Tämä RNA tulee säikeen ribosomeihin ja viruspartikkelin muiden proteiinien synteesi tapahtuu.
Virukset aiheuttavat erilaisia sairauksia. Virustaudit ovat hyvin erilaisia ja riippuvat virusten luonteesta, niiden virulenssista, tavoista päästä kehoon ja voittaa kehon luonnolliset suojaesteet. Infektio voi tapahtua ilman, ruoan, maidon, veden, eri esineiden, veren imevien niveljalkaisten (hyttysten, hyttysten ja punkkien) pureman kautta. Yksi solun luonnollisen puolustuksen tekijöistä viruksia vastaan on solujen tuottama interferoni, aine, joka luo solun vastustuskyvyn virukselle, vaikka tämä suojaava vaikutus on lyhytikäinen.
Interferoni on pienimolekyylipainoinen proteiini, jolla on antiviraalisia ominaisuuksia ja joka sisältää hiilihydraatteja, mukaan lukien glukosamiini. Avattu vuonna 1957. Isaac ja Lindenman. Interferonin tärkein ominaisuus on sen antiviraalinen vaikutus, joka ilmenee tarttuvien ja onkogeenisten virusten lisääntymisen estämisessä. Aktiivisin interferoni on ihmisen interferoni. Interferonilla ei ole valikoivaa antiviraalista aktiivisuutta ja se vaikuttaa lähes kaikkiin viruksiin.
Interferoni ei inaktivoi viruksia tai niiden nukleiinihappoja suoraan, ei häiritse viruksen adsorptiota ja tunkeutumista soluun eikä sen proteiinipitoisuutta. Interferoni vaikuttaa viruksen lisääntymisen solunsisäiseen vaiheeseen. Mekanismi, jolla interferoni on vuorovaikutuksessa solujen kanssa, joissa se indusoi viruslääkkeen, on edelleen epäselvä. Joidenkin kirjoittajien mukaan interferoni voi aiheuttaa virusten vastaisen tilan soluissa havaitsematta aktiivisuuden heikkenemistä, toisten mukaan interferonin suojaava vaikutus liittyy sen imeytymisen voimakkuuteen.
Interferonin vaikutus on sallittu sekä translaation että transkription tasolla. Ensimmäistä tukee data, jonka mukaan interferoni, vaikuttaen virusspesifisen RNA: n synteesiin, estää virusproteiinien synteesiä. Se ei ainoastaan vähennä syntyneiden virusspesifisten polypeptidien määrää tartunnan saaneissa soluissa, vaan myös lyhentää polypeptidiketjuja. Oletetaan, että interferoni voi muuttaa viruksen RNA: ta niin paljon, että se menettää kykynsä osallistua polysomien muodostumiseen.
Interferonin toiminnan kannattajat transkription tasolla luottavat tietoihin interferonin estävästä vaikutuksesta varhaisen virus -RNA: n transkriptioon. Tämä inhibitio liittyy viruksen indusoiman synteesin tukahduttamiseen, jota välittää virion-RNA-riippuvainen polymeraasi. Yleisin oletus on, että interferonille altistumisen seurauksena translaatio häiriintyy, mikä tekee mahdottomaksi suorittaa viruksen lisääntymisen seuraavat vaiheet.
On monia aineita, jotka edistävät interferonin muodostumista soluihin ja kudoksiin. Niitä kutsutaan interferonin indusoijiksi.
1. YLEISET MÄÄRÄYKSET
Näitä entsyymejä ovat esimerkiksi deoksytyleenikinaasit ja DNA -polymeraasit. Joten esimerkiksi soluun tunkeutuva asyloguanosiini (asykloviiri) fosforyloituu viruksen deoksitymidiinikinaasilla ja trifosfaatin muodossa estää herpes simplex -viruksen DNA -polymeraasia (enemmän kuin solun DNA -polymeraasi). Lisäksi tämä yhdiste on upotettu viruksen DNA: han. Ribaviriini toimii eri periaatteella: 5-trifosfaatin muodossa se estää erityisesti virusten RNA-polymeerisen DNA-transkriptaasin. Saadut tiedot ovat erittäin lupaavia uusien selektiivisesti vaikuttavien viruslääkkeiden luomiseksi.
Antiviraalisten aineiden toiminnan suunta voi olla erilainen. Se koskee viruksen ja solun välisen vuorovaikutuksen eri vaiheita. Tiedetään siis aineita, jotka toimivat seuraavasti:
Ne estävät viruksen adsorptiota soluun ja (tai) sen tunkeutumista soluun, samoin kuin virusgenomin (midontan, remantadine) vapautumisprosessia ("deproteinointia").
Ne estävät "varhaisten" virusproteiini-entsyymien (guanidiini) synteesiä.
Ne estävät nukleiinihappojen (tsidovudiini, asykloviiri, vidarabiini, idoksuridiini) synteesiä.
Ne estävät virionien "kokoonpanon" (metisatsoni).
Lisää solun vastustuskykyä virukselle (interferonit).
Jotkut lääkkeet on tarkoitettu lääketieteellisiin tarkoituksiin, toiset pääasiassa virusinfektioiden ehkäisyyn.
Midantaani (adamantanamiinihydrokloridi, amantadiini, viregit, symmetreeli) vaikuttaa mikroviruksiin, jotka ovat RNA -viruksia. Uskotaan, että midantaani estää viruksen kulkeutumisen isäntäsoluun ja estää myös viruksen genomin vapautumisen solussa. Imeytyy hyvin ruoansulatuskanavasta. Se erittyy pääasiassa munuaisten kautta.
Midantanin pääasiallinen käyttö on tyypin A2 influenssan ehkäisy. Lääkkeenä se on tehoton.
Midantaanilla voi olla kielteinen vaikutus keskushermostoon (yliherkkyys, uneliaisuus, vapina, ataksia). Dyspeptiset häiriöt, ihovauriot ovat mahdollisia. Remantadiinilla (rimantadiinihydrokloridi), joka on kemialliselta rakenteeltaan samanlainen kuin midantaani, on samanlaiset ominaisuudet ja käyttöaiheet.
Globaali ongelma on hankitun immuunipuutosoireyhtymän (AIDS) hoito. Sitä kutsutaan erityiseksi retrovirukseksi. AIDS -hoito edellyttää antiretroviraalisen, immunomoduloivan ja oireenmukaisen hoidon käyttöä. Antiviraalisista lääkkeistä käytetään vain atsidotymidiiniä (3-atsido-3-deoksitymidiini). Kaupallista lääkettä atsidotymidiiniä kutsutaan tsidovudiiniksi (atsidotymidiini, retroviiri). Tsidovudiinin toimintaperiaate on, että se fosforyloituna soluissa estää viruksen DNA -käänteistranskriptaasia. Lääke imeytyy hyvin. Biologinen hyötyosuus on noin 65%. Tunkeutuu hyvin veri-aivoesteen läpi. Noin 75% lääkkeestä metaboloituu maksassa (atsidotymidiiniglukoronidia muodostuu). Osa tsidovudiinista erittyy muuttumattomana munuaisten kautta (joidenkin tietojen mukaan 16-18%).
Zidovudine -hoito on aloitettava mahdollisimman aikaisin. Sen terapeuttinen vaikutus ilmenee pääasiassa ensimmäisten 6-8 kuukauden aikana. hoidon alusta. Valitettavasti tsidovudiini ei paranna potilaita, vaan vain viivästyttää taudin kehittymistä. Lisäksi retroviruksen lääkeresistenssi kehittyy sille. Tällä hetkellä etsitään laajasti uusia lääkkeitä ja rokotteita, joita tarvitaan pikaisesti aidsin erittäin epäsuotuisan epidemiologisen tilanteen muuttamiseksi. Tsidovudiinin sivuvaikutuksista ensisijassa ovat hematologiset häiriöt: anemia, neutropenia, trombosytopenia, pancythemia. Päänsärky, unettomuus, lihaskipu ja munuaisten toiminnan tukahduttaminen ovat mahdollisia. Merkittävä saavutus on erittäin tehokas antiherpeettinen aine, sykloviiri (Zovirax). Kemiallisesti johdettu hedaniinista. Asykloviiri fosforyloituu soluissa. Infektoiduissa soluissa asykloviiritrifosfaatilla on estävä vaikutus viruksen DNA -polymeraasiin. Noin 1/5 lisätystä aineesta imeytyy ruoansulatuskanavasta. Suurin pitoisuus kertyy 1-2 tunnin kuluttua. Biologinen hyötyosuus on noin 20%. Plasman proteiinit sitovat 12-15% aineesta. Läpäisee tyydyttävästi veri-aivoesteen.
Vidorobin (adeniini, arabinosidi) on myös tehokas viruslääke. Soluun tunkeutuva vidorobiini fosforyloituu. Estää viruksen DNA -polymeraasia. Tämä estää suurten DNA: ta sisältävien virusten replikaation. Elimistössä se muuttuu osittain arabinosidiksi, joka on vähemmän aktiivinen hypoksontiinivirusta vastaan.
Sitä käytetään menestyksekkäästi herpes -aivotulehdukseen (laskimonsisäisenä infuusiona), mikä vähentää tämän sairauden kuolleisuutta 30-75%. Joskus käytetään monimutkaisiin vyöruusuihin. Tehokas herpeettiseen pyrotokonjunktiviittiin.
IDoksuridiini (kerisidi, iduridiini, ofton-UDI), joka on tymidiinin analogi, sisällytetään DNA-molekyyliin. Tältä osin se estää tiettyjen DNA: ta sisältävien virusten replikaation. Idoksuridiinia käytetään paikallisesti herpes -silmätulehduksiin (keratiitti). Voi aiheuttaa ärsytystä, silmäluomien turvotusta. Se ei ole kovin sopiva resorptiiviseen toimintaan, koska lääkkeen toksisuus on merkittävä.
Metisatsonilla (mirboran) on voimakas antiviraalinen aktiivisuus. Se on tehokas isorokkovirusta vastaan. Vaikutusmekanismi liittyy ilmeisesti siihen tosiseikkaan, että metisatsoni häiritsee virionien kokoonpanoprosessia ja estää viruksen rakenneproteiinin synteesiä.
Lääkkeellä oksoliini on kohtalainen teho adenoviruksen keritokonjunktiviitissa, herpeettisessä keratiitissa ja eräissä virusinfektioissa.
Interferoneja käytetään myös virusinfektioiden estämiseen. Tämä on ryhmä biogeenisiä aineita, jotka liittyvät pienimolekyylipainoisiin glykoproteiineihin ja joita kehon solut tuottavat, kun ne altistuvat viruksille. Ne saavat solut vastustamaan virusten vaurioitumista. Interferoneja muodostuu virusinfektion alussa. Niille on ominaista laaja antiviraalinen kirjo (niillä ei ole spesifistä vaikutusta yksittäisiin viruksiin). Niillä on kuitenkin selvä lajispesifisyys suhteessa mikrobisoluihin. Interferoneja kutsutaan joskus laajakirjoisiksi viruslääkkeiksi. Resistenssi interferoneille viruksissa ei synny. Useita viikkoja toipumisen jälkeen interferoneja ei havaita veressä. Ne ovat käytännössä vaarattomia keholle. Saatavilla olevien tietojen mukaan herkistyminen ei yleensä aiheudu. Interferonit tunkeutuvat soluun ja sitoutuvat tiiviisti siihen. Ilmeisesti niiden antiviraalisen vaikutuksen mekanismi johtuu siitä, että ne aiheuttavat useiden entsyymien muodostumisen makroorganismin solujen ribosomeista, jotka estävät sekä RNA: ta että sen translaatiota virusproteiiniksi. Tämä johtaa viruksen lisääntymisen estämiseen. Interferonit eivät käytännössä läpäise veri-aivoestettä. Kliinisessä käytännössä käytetään ihmisen leukosyyttien (α-) ja fibroblastien (β-) interferoneja. Interferonia saadaan myös geenitekniikalla. Interferonin paikkaa virusinfektioiden hoidossa ei ole tarkasti määritetty. Interferonien enemmän tai vähemmän voimakas tehokkuus influenssan, herpeettisen keratiitin, ihon ja sukupuolielinten herpeettisten vaurioiden jne.
2. VIRUSTUSVÄLINEIDEN LUOMISHISTORIA
Ensimmäinen spesifiseksi viruslääkkeeksi ehdotettu lääke oli tiosemikarbatsoni, jonka virusisidisen vaikutuksen on kuvannut G. Domagk (1946). Tämän ryhmän lääkkeellä, tiosetotsonilla, on jonkin verran antiviraalista aktiivisuutta, mutta se ei ole riittävän tehokas; sitä käytetään tuberkuloosilääkkeenä. Tämän ryhmän johdannaisia 1, 4-bentsokinoni-guanyyli-hydratsinotio-semikarbatsoni nimellä "pharingosept" (faringosept, Romania) käytetään "kielellisten" (suuonteloon imeytyvien) tablettien muodossa tartuntatautien hoitoon ylemmät hengitystiet (tonsilliitti, stomatiitti jne.)
Myöhemmin syntetisoitiin metisatsoni, joka tukahdutti tehokkaasti isorokkovirusten lisääntymisen, ja vuonna 1959 - nukleosidi -idoksuridiini, joka osoittautui tehokkaaksi viruslääkkeeksi, tukahduttamalla herpes simplex -viruksen ja vaccinian (rokotustauti). Systeemisen käytön sivuvaikutukset rajoittivat idoksuridiinin laajan käytön mahdollisuutta, mutta se pysyi tehokkaana aineena paikalliseen käyttöön silmänhoidossa herpeettisen kerotiitin hoitoon. Idoksuridiinin jälkeen alkoi saada muita nukleosideja, joista tunnistettiin erittäin tehokkaita viruslääkkeitä, mukaan lukien asykloviiri, ribamidiini (riboviriini) ja muut. Vuonna 1964. Amantadiini (midantiini) syntetisoitiin, sitten rimantadiini ja muut adamantaanijohdannaiset, jotka osoittautuivat tehokkaiksi viruslääkkeiksi. Merkittävä löytö oli endogeenisen interferonin löytäminen ja sen antiviraalisen aktiivisuuden vahvistaminen. Nykyaikainen DNA: n rekombinaatiotekniikka (geenitekniikka) on avannut mahdollisuuden interferonien laajalle levinneeseen käyttöön virus- ja muiden sairauksien hoidossa ja ehkäisyssä.
Merkittävä tapahtuma oli endogeenisen interferonin löytäminen ja sen antiviraalisen aktiivisuuden vahvistaminen. Vuoteen 1957 asti interferoneja pidettiin uteliaana biologisena ilmiönä. Vuosina 1957 - 1967 tutkittiin interferonin yleisiä tuotanto- ja vaikutusmalleja. Tämän työn aikana vahvistettiin tämän selkärankaisten (kaloista ihmisiin) solujen tämän proteiinin muodostumisen ilmiön yleismaailmallisuus ja kehitettiin tärkeimmät menetelmät sen tuottamiseksi ja puhdistamiseksi.
Vuonna 1967 todettiin suurimolekyylisten kaksijuosteisten RNA: iden johtava rooli interferonin indusoinnissa ja aloitettiin aktiivisimpien lääkkeiden etsiminen, joilla on mahdollisuus kliiniseen käyttöön.
Seuraavien 13 vuoden aikana (1967 - 1980) tutkittiin interferonin ja sen indusoijien antitogeenistä vaikutusta, interferonin superinduktion periaatteet todistettiin kokeellisesti. Samana ajanjaksona monimutkaisen monikomponenttisen tuotantomekanismin olemassaolo ja interferonin vaikutus todettiin teoreettisesti, mikä myöhemmin johti geenien ja informaatio -RNA: iden tunnistamiseen interferonille ja entsyymeille, jotka suorittavat sen toimintaa. 80 -luvulla leimasivat tällaiset suuret tapahtumat interferonin ja sen indusoijien tutkimuksessa:
1) interferonijärjestelmän oppi on vihdoin muotoutunut;
2) geenitekniikan menetelmien avulla saatiin lupaavia kliiniseen käyttöön tarkoitettuja interferonivalmisteita;
3) interferonigeenien moninaisuus on osoitettu (ihmisillä niiden määrä on lähellä 30);
4) tunnistetut käyttöaiheet ja vasta -aiheet interferonien ja niiden indusoijien kliiniselle käytölle.
80-90 -luvulla todettiin, että useiden immunostimuloivien ja antiviraalisten aineiden (prodignosaani, poludaani, arbidoli jne.) Vaikutus liittyy niiden interferogeeniseen aktiivisuuteen eli kykyyn edistää endogeenisen interferonin muodostumista.
Kotimaiset tutkijat ovat kehittäneet useita synteettisiä ja luonnollisia (kasviperäisiä) lääkkeitä systeemiseen ja paikalliseen käyttöön virussairauksissa (bonaftoni, arbidoli, oksoliini, deityformiini, tebrofeeni, alpitsariini jne.). Nyt on todettu, että useiden immunostimuloivien ja antiviraalisten aineiden vaikutus liittyy niiden interferoniaktiivisuuteen, ts. kyky stimuloida endogeenisen interferonin muodostumista.
Kronologinen taulukko virusten vastaisista tapahtumista
| Vuosi | Tapahtuma |
| 1946 | Tiosemikarbatsonia ehdotettiin viruslääkkeeksi. Toiminnan kuvasi G. Domagk |
| 50 -luku | Metisazon on auki |
| 1957 | Isaacs ja Lindenman löysivät interferonin |
| 1957–1967 | Interferonin yleisiä tuotanto- ja vaikutusmalleja on tutkittu. Kaikkien selkärankaisten solujen (kaloista ihmisiin) solujen muodostaman ilmiön yleismaailmallisuus on vahvistettu ja tärkeimmät menetelmät sen tuottamiseksi ja puhdistamiseksi on kehitetty. |
| 1959 | Löytyi idoksuridiini herpes simplex -virusta vastaan |
| 1964 | Syntetisoitu adamantaani, sitten rimantadiini ja muut adamantaanijohdannaiset |
| 1970 | Löytyi tiloroni, interferoni -induktori |
| 1967-1980 | Interferonin ja sen indusoijien antitogeenistä vaikutusta tutkittiin, interferonin superinduktion periaatteet todistettiin kokeellisesti. |
| 80-90 vuotta | On osoitettu, että useiden immunostimuloivien ja antiviraalisten aineiden (prodignosaani, poludaani, arbidoli jne.) Vaikutus liittyy niiden interferogeeniseen aktiivisuuteen eli kykyyn edistää endogeenisen interferonin muodostumista |
3. Antiviraalisten aineiden luokittelu
Antiviraalisten aineiden toiminnan suunta voi olla erilainen. Se koskee viruksen ja solun välisen vuorovaikutuksen eri vaiheita. Tiedetään siis aineita, jotka toimivat seuraavasti:
estävät viruksen adsorptiota soluun ja sen tunkeutumista soluun sekä viruksen genomin vapauttamisprosessia. Näitä ovat lääkkeet, kuten midantaani ja rimantadiini;
estävät varhaisten virusproteiinien synteesiä. Esimerkiksi guanidiini;
estää nukleiinihappojen (tsidovudiini, asykloviiri, vidarabiini, idoksuridiini) synteesiä;
estävät virionien "kokoonpanon" (metisatsoni);
lisätä solujen vastustuskykyä virukselle (interferonit)
Se esitteli viruslääkkeiden luokituksen toimintamekanismin mukaan.
Rakenteen mukaan viruslääkkeet voidaan jakaa:
1. Adamantaanijohdannaiset (midantaani, rimantadiini)
2. Nukleosidianalogit (tsidovudiini, asykloviiri, vidarabiini, idoksuridiini)
3. Tiosemikarbatsonin johdannaiset - metisatsoni
4. Makro -organismin (interphyron) solujen tuottamat biologiset aineet
Mutta on ymmärrettävämpää, että viruslääkkeet jaetaan sairauden tyypistä riippuen ryhmiin:
1. influenssan vastaiset lääkkeet (remantadiini, oksoliini jne.)
2. Antiherpeettinen ja antisytomegalovirus (tebrofeeni, riodoksoni jne.)
3. Ihmisen immuunikatovirukseen vaikuttavat lääkkeet (atsidotymidiini, fosfaniformiaatti)
4. Lääkkeet, joilla on laaja vaikutusalue (interferonit ja interferonogeenit)
Mashkovsky M.D. luotu seuraava viruslääkkeiden luokitus:
A) Interferoni
interferoni. Ihmisen luovuttajan veren leukosyyttien interferoni.
lukitus. Puhdistettu a-interferoni, joka on saatu luovutetusta verestä.
referoni. Rekombinantti a2-interferoni, jonka tuottaa Pseudomonas-bakteerikanta, jonka geneettiseen laitteeseen on lisätty ihmisen leukosyyttien a2-interferonin geeni.
introni A. Rekombinantti interferoni alfa-2c.
beetaferoni. Rekombinantti ihmisen β1-interferoni.
Interferonin induktorit
keskipäivä. Jauhe tai huokoinen massa valkoinen, jolla on immunostimuloiva vaikutus, ts. kyky stimuloida endogeenisen interferonin tuotantoa ja sillä on antiviraalinen vaikutus.
neovir. Toiminta on sama kuin poludanilla.
B) Amantadiinin ja muiden synteettisten yhdisteiden ryhmien johdannaiset
Remantadiini. Sitä käytetään parkinsonismilääkkeenä, joka osoittaa ennaltaehkäisevän toiminnan tiettyjen viruskantojen aiheuttamaa influenssa -infektiota vastaan.
Adapromiini. Lähellä remantadiinia.
Deytiforin. Samanlainen kuin remantadiini.
Arbidol. Antiviraalinen lääke, joka estää influenssa A- ja B -viruksia.
Bonafton. Sillä on antiviraalinen vaikutus herpes simplex -virusta ja joitakin adenoviruksia vastaan.
Oxolin. Sisältää virusidaalista aktiivisuutta, on tehokas silmien, ihon, viruksen nuhan virussairauksissa; on ennaltaehkäisevä vaikutus influenssaa vastaan.
Tebrofeeni. Sitä käytetään voiteena silmäsairauksiin, virusinfektioihin tai virusperäisen ihosairauden hoitoon, ja sitä voidaan käyttää myös lasten litteiden syylien hoitoon.
Ryodoxol. Sillä on antiviraalinen optimaalisuus ja sillä on antifungaalinen vaikutus.
Florenal. Avaa neutraloivan vaikutuksen viruksia vastaan.
Metisazon. Tukahduttaa pääryhmän viruksen lisääntymistä: sillä on ennaltaehkäisevä vaikutus isorokovirusta vastaan ja se helpottaa rokotuksen jälkeisten komplikaatioiden kulkua, viivästyttää ihoprosessin leviämistä ja edistää kuohuviinien nopeampaa kuivumista. On todisteita metisatsonin tehokkuudesta toistuvan sukupuolielinten herpesin hoidossa.
V) Nukleosidit
Idoksuridiini. Käytetään silmätulehduksessa keratiitin hoitoon.
Asykloviiri. Tehokas herpes simplex -viruksia ja herpes zosteria vastaan. Sillä on immunostimuloiva vaikutus.
Ganciclovir. Asykloviiriin verrattuna gansikloviiri on tehokkaampi ja lisäksi se vaikuttaa paitsi herpesvirukseen myös sytomegalovirukseen.
Famsikloviiri. Sillä on samat toiminnot kuin gansikloviirilla.
Ribamidiili. Ribamidiililla, kuten asykloviirilla, on antiviraalinen vaikutus. Estää virus -DNA: n ja RNA: n synteesiä.
Tsidovudiini. Antiviraalinen lääke, joka estää retrovirusten, mukaan lukien ihmisen immuunikatovirus (HIV), replikaation.
G) Kasviperäiset viruslääkkeet
1.Flakosidi. Se saadaan Amur rue -perheen sametin lehdistä. Lääke on tehokas DNA -viruksia vastaan.
Alpidariini. Johdettu yrtistä Koneermena alpine ja keltaisesta penniä, palkokasvien perheestä. Tehokas herpes-ryhmän DNA: ta sisältäviä viruksia vastaan. Estovaikutus herpes simplex -viruksen lisääntymiseen ilmenee pääasiassa viruksen alkuvaiheessa.
Cholepin. Puhdistettu uute osasta mepedetsi -kasvia kauniista penniäisistä, palkokasveista. Sillä on antiviraalinen aktiivisuus herpes-ryhmän DNA: ta sisältäviä viruksia vastaan.
Ligosin. Käytetään herpes -ihosairauksiin.
Gossypol. Tuote, joka on saatu puuvillansiementen käsittelystä tai puuvillan juurista, malvaceous -perhe. Lääke on aktiivinen eri viruskantoja vastaan, mukaan lukien herpesviruksen dermatotrooppiset kannat. Vaikuttaa heikosti grampositiivisiin bakteereihin.
4. BIOLOGISEN TOIMINNAN MEKANISMI
4.1. Influenssan vastaiset lääkkeet
Kaikki tämän ryhmän lääkkeet suojaavat ihmissoluja influenssaviruksen tunkeutumiselta niihin, koska estää viruksen sitoutumiskohdat solukalvon pinnan kanssa. Ne eivät vaikuta soluihin tunkeutuneisiin viruksiin, joten niitä käytetään influenssan yksilölliseen tai massiiviseen ehkäisyyn henkilöillä, jotka ovat kosketuksissa potilaiden kanssa tai epidemian aikana. Kaikki lääkkeet (paitsi oksoliini) määrätään suun kautta. Ne imeytyvät hyvin ruoansulatuskanavasta. Hyvin pienessä osassa ne sitoutuvat veriplasman proteiineihin, tunkeutuvat hyvin kaikkiin kudoksiin ja nesteisiin, myös aivo -selkäydinnesteeseen. Eliminaatio tapahtuu osittain maksassa, mutta pääasiassa munuaisissa (90%). Siksi potilailla, joilla on munuaisten vajaatoiminta, lääkkeiden toistuva antaminen voi johtaa kumulaatioon ja siihen voi liittyä haittavaikutuksia.
4.2. Antiherpeettiset ja sytomegaloviruslääkkeet
Antiherpeettinen (tebrofeeni, riodoksoli, idoneuridiini, vidarabiini, ocyclovir, valacyclovir). Sytomegalovirus (gansikloviiri, fosfonoformaatti).
Kaikki nämä lääkkeet estävät replikaation, ts. häiritä viruksen nukleiinihappojen synteesiä. Vidarabiinia käytetään paikallisesti, ja jos herpesinfektio (enkefaliitti) vähenee, se annetaan laskimonsisäisesti. Mutta lääke on huonosti liukoinen, joten sen infuusio suuressa määrässä nestettä kestää noin 12 tuntia, mikä ei ole toivottavaa potilaalle, jolla on enkefaliitti, aivoturvotus. Vidarabiinin käyttö veri-aivoesteen läpi on noin 30% lääkeaineen pitoisuudesta veriplasmassa.
Maksassa lääke muuttuu arabinosiinihypoksantiiniksi, tämä metaboliitti pysyy aktiivisena ja jakautuu nopeasti kudoksiin. Eliminaatio tapahtuu virtsassa (50%) ja ulosteessa. Acyclovir, valacyclovir, ganciclovir määrätään suun kautta aterioiden aikana ja annetaan myös lihaksensisäisesti ja suonensisäisesti.
Bioabsorptio ruoansulatuskanavasta on 15-20%, mutta tämä riittää vaikutuksen aikaansaamiseksi. Lääkkeillä on korkea aktiivisuus, ja niillä on kyky kerääntyä valikoivasti viruksen tartuttamiin soluihin, mutta ei ehjiin soluihin. Plasman proteiineihin sitoutuminen on vain 9-30%, joten lääkkeet tunkeutuvat hyvin eri kudoksiin ja nesteisiin. Ihmiskehossa valacyclovir muuttuu nopeasti ja melkein kokonaan asykloviiriksi ja valiiniksi valacyclovir hydrolase -entsyymin vaikutuksesta. 10-15% asykloviirista ja gansikloviirista tapahtuu biotransformaatiossa maksassa. Suurin osa lääkkeistä (80-90%) muuttumattomana ja 9 -karboksimetoksimetyyliguaniinin metaboliittina erittyy munuaisten kautta.
4.3. Ihmisen immuunikatovirukseen (HIV) vaikuttavat lääkkeet (tsidovutsiini, fosfonoformaatti)
Lymfotrooppisen HIV: n tunkeutumisen jälkeen lymfosyyttiin viruksen DNA syntetisoidaan matriisille (viruksen RNA) käänteiskopioijaentsyymin (käänteistranskriptaasi) vaikutuksesta, mikä johtaa lymfosyyttien vaurioitumiseen. Areredotymidiinin ja fosfonoformiitin vaikutusmekanismi on nimetty entsyymi. Yleensä lääkkeet ovat tehokkaita viruksen kantajissa ennen sairauden merkkien ilmaantumista. Näiden lääkkeiden lisäksi nyt on ilmestynyt uusia antiretroviraalisia lääkkeitä: dideoksimetysiini ja dideoksisidiini. Atsidovudiini annetaan suun kautta tai laskimoon. Biologinen hyötyosuus ruoansulatuskanavasta on 60%. Yhteys veriplasman proteiineihin 35%. Atsidotymidiini tunkeutuu helposti eri kudoksiin ja nesteisiin, mukaan lukien aivo -selkäydinneste. Se muuttuu biotransformaatiossa maksassa, ja sen päämetaboliitti on 5 | -o -glukuronidi. Erittyminen - munuaisten avulla muuttumattomana (90%) ja metaboliittien muodossa.
4.4. Laajakirjoiset viruslääkkeet (interferonit)
Interferonin indusoijien (lukuisat synteettiset ja luonnolliset aineet) vaikutuksesta suoritetaan induktio, jonka tuloksena on interferonigeenien masennus, jotka ovat lokalisoituneet ihmisen 2., 9. ja mahdollisesti 5. ja 13. kromosomiin. Vastauksena induktioon interferonin muodostuminen, synteesi tapahtuu ihmiskehon soluissa.
Tärkein indikaattori interferoni-induktorien aktiivisuudesta on ns. "Seerumin tarkan" interferonin tuotanto veressä.
Kun indusoijia annetaan enteraalisesti kehoon, interferonivaste saadaan ruoansulatuskanavan lymfosyyttikudoksen GALT -järjestelmän lymfosyyteistä (erytrosyytteistä), jotka on konsentroitu Walder -renkaan, höyhenplakkien, limakalvon mononukleaarien ja elimistön memfosyyttien muodossa ohutsuolesta ja lisäyksestä, jossa ne voivat toimittaa väestölle erikoistuneet kalvosolut, jotka kykenevät kuljettamaan makromolekyylejä ohutsuolen seinämästä epiteelisuojan läpi. Suurin osa tässä tapauksessa tuotetusta interferonista voidaan hyödyntää paikallisesti ympäröivillä suoliston soluilla, eikä se saavuta kiertävää verta (parakriinityyppi). Toinen osa tuotetusta interferonista tulee vereen joko suoraan kudosnesteestä (endokriininen tyyppi) tai vaeltavien lymfomonosyyttien ja makrofagien kautta. Interferonin tuotanto suolistossa ylittää ja ylittää sen muodostumisen tason muissa elimissä.
Kun suun kautta annetaan suurimolekyylipainoisia interferonin indusoijia, jotka on suljettu liposomeihin (polyguacil, larifan), maksasta tulee interferonin, eli hepatosyyttien ja Kupffer-solujen, muodostumisen hallitseva paikka. Vaikka tässä tapauksessa suolisto on indusoijan ensimmäinen vuorovaikutuskeho kehon kanssa, sitä syntetisoidaan merkittävä määrä interferonia, mutta liposomeissa yli 80% indusoijasta kuljetetaan maksaan, joten interferonin tuotanto tässä elimessä on 2-4 kertaa suurempi kuin suolistossa.
Näin ollen, kun interferonin indusoijat saapuvat kehoon ja seerumin interferonin tuotanto elimistössä, elimet tuottavat itsenäisen, paikallisen interferonin tuotannon. Tässä tapauksessa johtava rooli interferonin tuotannossa on määritetään yhtä lailla sekä interferonin induktioreitillä että induktorin koostumuksella ja siten interferonikompetenttien solujen herkkyydellä käytetylle indusorille.
Interferonin muodostumisen jälkeen elimissä se tulee verenkiertoon ja liittyy niin kutsuttuun "seerumin" interferoniin (syntetisoitu veressä, seerumi induktorien vaikutuksen alaisena). Interferonin muita antiviraalisia vaikutuksia voidaan esittää kaaviona.
4.5. Amiksin - mahdollisuudet ja näkymät soveltamiseen kliinisessä käytännössä
Uusien farmakologisten aineiden etsiminen ja tutkiminen on yksi nykyaikaisen lääketieteen tärkeimmistä ongelmista. Menestys uuden lääkkeen valmistuksessa on seurausta maailmanlaajuisesta pitkän aikavälin strategiasta. Samaan aikaan mahdollisuudet uuden lääkkeen luomiseen liittyvän työn onnistuneeseen saattamiseen päätökseen ovat hyvin pienet, noin 1 000: sta 100 000: een, ja uuden lääkkeen kehittämis- ja markkinointiprosessi kestää 12–15 vuotta.
Uusien lääkkeiden kehittäminen 2000-luvun sairauksia vastaan on LENS-Pharmin ensisijainen toiminta-alue. Erityisen kiinnostavia ovat lääkkeet, jotka lisäävät kehon vastustuskykyä tartuntatekijöille. Yksi näistä lääkkeistä on Amiksin.
INTERFERON -JÄRJESTELMÄN TOIMINTAJÄRJESTELMÄ
Amiksinin tie kliiniseen käytäntöön sisälsi useita peräkkäisiä vaiheita lupaviranomaisten läpikäymisessä. Kaikki tehon ja turvallisuuden parametrit on dokumentoitu alkutilasta aina kokeellisen hoidon aikana tehtyihin mittauksiin (annosmuoto, antotapa, antotapa, annoksen valintasuunnitelma, hoidon kesto). Tähän mennessä on muodostunut ajatus mahdollisista tehokkaista Amiksin -hoitokursseista ja niiden tarpeesta ennen kaikkea sairauksille, joiden hoitoon ja ehkäisyyn ei ole tyydyttäviä menetelmiä. Samalla selvitettiin valittujen sairauksien vaikutus potilaisiin ja koko yhteiskuntaan, nykyisiin hoitomenetelmiin sisältyvät haitat, Amiksinin ominaisuudet minkä tahansa käytettävissä olevan hoitomenetelmän parantamiseksi. Taloudellinen arviointi perustui vertailutietoihin vaihtoehtoisiin toimiin. Erityistä huomiota kiinnitettiin kysymyksiin vastaamiseen siitä, kuinka paljon potilaalle ja / tai yhteiskunnalle halutun tuloksen saaminen maksaa. Todisteet Amiksinin terapeuttisten ja ennaltaehkäisevien kykyjen tehokkuudesta ja taloudellisesta toteutettavuudesta olivat perusta lääkkeen sisällyttämiselle hoito- ja ehkäisystandardeihin sekä korvaus Amiksin -hoidon kustannuksista sellaisten sairauksien kuin virushepatiitin, influenssa ja muut akuutit hengitystieinfektiot, verenvuotokuume.
Oli erittäin tärkeää luoda tieto- ja analyyttinen kokoelma tutkimustulosten perusteella. Kun yleistettiin Amiksinin käyttökokemusta, ratkaiseva rooli annettiin muodollisille menetelmille, mikä mahdollisti johdonmukaisimpien suositusten laatimisen todellista käytäntöä varten. Tässä kokoelmassa esitettyjen tietojen arvon määrää toisaalta johtavien tutkijoiden ja asiantuntijoiden tunnustama tieteellinen pätevyys ja toisaalta yhteys Amiksinin tarkoituksellisen ja järkevän käytön ongelmien ratkaisuun todellinen käytäntö.
4.5.1. Amiksin -lääkkeen nimi ja kuvaus
Rekisterinumero 96/252/1; 96/252/3.
Kansainvälinen ei -kaupallinen nimi - Tiloron(2,7, -bis-9h-fluoreeni-9-onidihydrokloridi).
Pienimolekyylipainoinen synteettinen aromaattinen yhdiste, joka kuuluu fluorenonien luokkaan.
6 ja 10 kappaleen kalvopäällysteiset tabletit pakkauksessa, annos 0,125 g (aikuinen) ja 0,06 g (lapsi)
4.5.2. Antiviraalinen aktiivisuus ja interferonia tuottavien solujen induktio.
Amiksinilla on antiviraalinen vaikutus monenlaisia viruksia vastaan.
Amiksin indusoi sekä ensimmäisen (alfa-, beeta-) että toisen (gamma) -tyypin interferonin muodostumista.
Amiksin "käynnistää" interferonin synteesin, toisin kuin polyklonaalinen induktio tietyissä solupopulaatioissa.
Interferonin induktio suoritetaan ilman apusoluja, mikä on osoitettu kokeilla puhtaalla viljelmällä, erityisesti T -soluilla.
Vaikutuksen voimakkuuden ja keston suhteen Amiksinilla on indusoijien parhaat ominaisuudet: myöhäisen interferonin "tuotanto", suurin vasteaika on 10-18 tuntia.
4.5.3. Vaikutukset immuunijärjestelmään ja tulehdukseen.
Ilmentyminen HLA-luokan 1 molekyylien, HLA-DR-luokan 2 antigeenien solukalvoilla.
NK -solujen kasvu ja aktivointi.
Vasta -aineiden toiminnallisen hyödyllisyyden palauttaminen.
Kohdennettu polarisaatio Th0 Th1.
Tulehdusvasteen mallintaminen tulehdusvaiheen mukaan.
4.5.4. Farmakokinetiikka
Imu. Oraalisen annon jälkeen Amiksin imeytyy nopeasti maha -suolikanavasta.
Jakelu. Biologinen hyötyosuus on 60%, noin 80% lääkkeestä sitoutuu plasman proteiineihin.
Erittyminen. 99% lääkkeestä erittyy muuttumattomana, puoliintumisaika on 48 tuntia.
4.5.5. Prekliiniset tutkimukset lääkkeen antiviraalisesta aktiivisuudesta
Amiksinin antiviraalista aktiivisuutta arvioitiin laboratorioeläimillä, jotka olivat tartunnan saaneet verenvuotokuumeen ja munuaisten oireyhtymän (HFRS) aiheuttavalla aineella, Hantaan -viruksella. Käytimme ennaltaehkäiseviä, terapeuttisia ja ennaltaehkäiseviä ja terapeuttisia menetelmiä lääkkeen antamiseksi valkoisille hiirille. Amiksinin suurin antiviraalinen aktiivisuus todettiin käytettäessä terapeuttista ja ennaltaehkäisevää suun kautta annettavaa annosta 10 mg / kg.
Amiksinin antiviraalista aktiivisuutta ja sen vaikutusta interferonin tilaan hepatiitissa tutkittiin 16-18 g painavilla urospuolisilla epälineaarisilla hiirillä. Virus (kanta Mescherina) läpäisi valkoisten hiirien vatsaontelonsisäisen infektion. Enteraalisen hepatiitin toistamiseksi hiirille injektoitiin suun kautta 0,2-0,3 ml 30-40%: n tartuntaa saaneiden eläinten maksan suspensiota fysiologisessa suolaliuoksessa. 1-7 päivää ennen tartuntaa koeryhmän eläimille annettiin suun kautta Amiksin-annos 4 mg. Eläimiä tarkkailtiin 14 päivän ajan. Yksi 4 mg amiksiinin injektio tarjosi 40-50% eläimille suojan hiirien enteraaliselta infektiolta 72 tunnin kuluessa lääkkeen antamisesta.
Amiksinin ennaltaehkäisevää ja terapeuttista vaikutusta 0,25 g painokiloa kohti Länsi -Niilin virusta vastaan tutkittiin kokeissa valkoisilla hiirillä. Amiksinin ennaltaehkäisevä anto johti koeryhmän kuolleisuuden vähenemiseen keskimäärin 23,4%.
5. ANTIVIRAALISTEN LÄÄKKEIDEN HANKINTA
Uudet reitit tiloronihydrokloridin synteesille
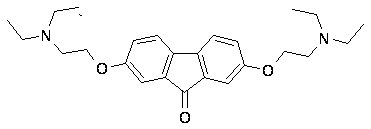
(2,7-bis-fluoren-9-oni
Syntetisoitu kahdella tavalla tiloroni-2,7-bis [(dietyyliamino) etoksi] fluorenoni-9 (I)
Fluorenoni-9 (II) HNO3: n nitrauksella saatiin 2,7- (O2N) 2-II (sp. 289-91 °), pelkistetty ZnCl2: lla HCl: ssa ja AcOH: ssa 2,7- (H2N) 2-II: ksi (sp. 287-9 °), jonka diatsotointi NaN02: lla 50% HBF4: ssä tuotti bis-diatsoyhdisteen (III), joka muutettiin 50% H2S04: n vaikutuksesta 2,7- (HO) 2-III: ksi (IV, sp. 320- 2 °). Fluoreeni (V) AcCl: n ja AlCl3: n asetylointi syntetisoi 2,7-Ac2-V (sp. 180-2є), joka muutetaan 3-ClC6H4COOOH: n vaikutuksesta F3CCOOH: n läsnä ollessa 2,7- (AcO) 2-V (VI) ) hapetettu Na2Cr207: lla AcOH: ssa 2,7- (AcO) 2-II (VII): ksi. IV: n tai VII: n vuorovaikutus KOH: n ja Et2NCH2CH2Cl * HCI: n kanssa antoi I.
0,099 mol 85-prosenttista 3-ClC6H4COOOH: a lisätään jäähdytettyyn seokseen, jossa on 0,037 mol 2,7-Ac2-V: tä, 400 ml HLF: ää ja 0,3 ml F3CCOOH: ta, suojattu valolta, lämmitetty 20 ° C: seen, pidetty kolme päivää , kloroformiliuos pestään kylläisellä Na2C03 -liuoksella ja kylläisellä NaCl -liuoksella, orgaaninen kerros kuivattiin vedettömällä MgS04: llä, suodos haihdutettiin, jolloin saatiin IV, saanto 62%, sp. 165-7єС (МеОН - хлф1).
0,034 mol VI: tä, 0,01 mol Na2Cr207 * 2H20: ta, 30 ml AcOH: ta keitetään 45 minuuttia, liuos jäähdytetään, lisätään 50 ml vettä, VII eristetään, saanto 53%, joten pl. 224,5-6,5є (SP).
0,04 mol Et2NCH2CH2Cl * HCl, 0,08 mol KOH, 0,01 mol IV tai VII 0,5 g PhCH2NMe3Br, 200 ml tolueenia ja 50 ml vettä keitetään 24 tuntia, jäähdyttämisen jälkeen, orgaaninen kerros erotetaan, pestään vedellä, kylläisellä NaCl -liuoksella ja kuivattiin vedettömällä MgS04: llä, tolueeni haihdutettiin tyhjössä, öljy liuotettiin 5 ml: aan MeOH: ta, lisättiin 50 ml: aan eetteriä. tyydyttymätön HCl. Jaa di-HG (I) 50%, joten pl. 232-4 ° (iso-PrOH-MeOH, 3: 1).
Bonaftonin saaminen (6-bromi-1,2-naftokinoni)
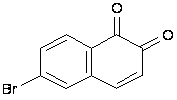
Herpesvirus vuosia, vuosikymmeniä ei välttämättä ilmene missään. Se integroituu soluihin, mukaan lukien hermosolut ja verisolut. Tästä syystä tavalliset immuunipuolustusmenetelmät eivät toimi.
Tiettyjä menestyksiä on saavutettu hengityselinsairauksien ehkäisyn ongelman ratkaisemisessa. Tämän ongelman ratkaisemisen monimutkaisuus liittyy suureen määrään tartuntatauteja, jotka aiheuttavat hengityselinsairauksia.
Interferoniluokat: luonnossa esiintyvät ja keinotekoisesti syntetisoidut. Menetelmät ihmisen leukosyyttien interferonin saamiseksi luovuttajan veren leukosyyteistä ja mikrobiologinen synteesi. Interferonien vaikutusmekanismit, terapeuttinen käyttö.
Interferonijärjestelmä (IF) on erottamaton osa immuunijärjestelmää ja varmistaa immuniteetin efektorisolujen lisääntymisen, erilaistumisen ja aktivoitumisen koordinoinnin. ...
LUOKITUS
A. Toimintamekanismin mukaan.
I. Aineet, jotka estävät viruksen adsorptiota ja tunkeutumista soluun.
1.Adamantanamines (Amantadine - "PK -Merz", Rimantadine - "Remantadin®", Tromantadine - "Viru -Merz serol").
2. Kasvi- ja eläinperäiset keinot (normaali ihmisen immunoglobuliini, glysyrritsiinihappo).
II Synteesiä estävät lääkkeet nukleiinihapot.
1. DNA -synteesiin vaikuttavat nukleotidit ja nukleosidit (asykloviiri, Valacyclovir, Ganciclovir, Famciclovir, Ribavirin, Cytarabin).
2.Nukleotidit ja nukleosidit - käänteiskopioijaentsyymin estäjät (abakaviiri, didanosiini, tsidovudiini, lamivudiini, stavudiini, telbivudiini, tenofoviiri, fosfosidi, entekaviiri).
3. Ei-nukleosidiset käänteiskopioijaentsyymin estäjät (Nevirapine, Etravirine, Efavirenz).
4.Neuroaminidaasin estäjät (Oseltamiviiri - "Temiflu », Zanamivir - "Relenza").
5. TMF: n estäjät - proteaasit (atatsanaviiri, darunaviiri, indinaviiri, ritonaviiri, lopinaviiri + ritonaviiri, nelfinaviiri, sakvinaviiri, telapreviiri, fosamprenaviiri).
6. Lääkkeet, jotka estävät DNA -polymeraasia ja käänteistranskriptaasia - fosfonihapon johdannaiset (Phosphozide -Nikavir).
III Lääkkeet, jotka estävät myöhäisten proteiinien synteesiä.
1. Tiosemikarbatsonijohdannaiset (metisatsoni - puuttuu tällä hetkellä GRLS: stä).
2. 5 -oksindolin johdannaiset (Umifenovir - "Arbidol").
IV Ei -spesifiset viruslääkkeet.
1. interferonit (IFN)
1.1 IFN alfa -2a: Roferon -A (ratkaisu p / c: lle.). jne
1.2 IFN alfa-2b: Grippferon (korkki.) Interferal ® (aerosoli paikalliseen käyttöön) jne.
1.3 IFN-beeta-1a: Avonex (lyof. d / liuos / m johdanto.) jne.
1.4 IFN -beeta -1b: Betaferon (lyof. d / r-ra d / in.), Ronbetal (ratkaisu p / c: lle.), Extavia (lyof.d / suspensio ihon alle) jne.
2. Interferonien induktorit
Penttaanidihapon imidatsolyylietanamidi - Ingaviriini; Meglumiiniakridoniasetaatti - Cycloferon; Tetrah- "alpitsariini"; "Kagocel"; Alfa-glutamyylitryptofaani + askorbiinihappo + bendatsoli-"Citovir-3" jne.
Antiviraalisen aktiivisuuden spektrin mukaan:
1. Media akuutin hengitystieinfektion ja influenssan hoitoon
1.1. M2 -kanavan salpaajat - adamantaanijohdannaiset: (Amantadiini - "PK -Merz", Rimantadiini - "Remantadin®", Tromantadiini - "Viru -Merz seroli").
1.2. Neuroaminidaasin estäjät: Oseltamiviiri - "Temiflu », Zanamivir - "Relenza".
1.3. Muut: Interferoni alfa -2b - "Grippferon", "Interferal®"; Penttaanidihapon imidatsolyylietanamidi - Ingaviriini; Meglumiiniakridoniasetaatti - Cycloferon; Tetrah- "alpitsariini"; "Kagocel"; Alfa-glutamyylitryptofaani + askorbiinihappo + bendatsoli-"Cytovir-3" ja muut interferonin induktorit.
2. Keinot vaikuttavat herpesvirusta vastaan
2.1. Herpes simplex -virus: Nukleotidit ja nukleosidit, jotka vaikuttavat DNA: n synteesiin (asykloviiri, Valacyclovir, Ganciclovir, Famciclovir, Ribavirin, Cytarabin); Tetrah- "alpitsariini"; interferoni alfa-2b.
2.2. Varicella zoster -virus
Ensisijainen akuutti infektio (vesirokko) - nukleotidit ja nukleosidit, jotka vaikuttavat DNA -synteesiin (Acyclovir, Valacyclovir, Ganciclovir, Famciclovir, Ribavirin, Cytarabin), tromantadiini - Viru -Merz serol.
Piilevä infektio (herpes zoster) - nukleotidit ja nukleosidit, jotka vaikuttavat DNA: n synteesiin (asykloviiri, Valacyclovir, Ganciclovir, Famciclovir, Ribavirin, Cytarabin); Tromantadiini - Viru -Merz Serol; Tetrah- "alpitsariini"; natriumdeoksiribonukleaatti rautakompleksilla - "Ferrovir"; interferoni alfa-2b, interferoni beeta-1b.
2.3. Sytomegalovirus - nukleotidit ja nukleosidit, jotka vaikuttavat DNA -synteesiin (Acyclovir, Valacyclovir, Ganciclovir, Famciclovir, Ribavirin, Cytarabin); interferoni -b.
3. Keinot HIV -infektion hoitoon
3.1. Käänteiskopioijaentsyymin estäjät
Nukleotidit ja nukleosidit - käänteiskopioijaentsyymin estäjät (abakaviiri, didanosiini, tsidovudiini, lamivudiini, stavudiini, telbivudiini, tenofoviiri, fosfosidi, entekaviiri).
Ei-nukleosidiset käänteiskopioijaentsyymin estäjät (nevirapiini, etraviriini, efavirentsi).
3.2. TMF: n estäjät - proteaasit (atatsanaviiri, darunaviiri, indinaviiri, ritonaviiri, lopinaviiri + ritonaviiri, nelfinaviiri, sakvinaviiri, telapreviiri, fosamprenaviiri).
4. Keinot, jotka vaikuttavat hepatotrooppisiin viruksiin (ks. Edellä interferonien luokittelu).
Interferonin (ifn) antiviraalisen vaikutuksen mekanismi
Indusoi solun antiviraalisen tilan (vastustuskyky virusten lisääntymiselle tai estämiselle)
· Estää viruksen mRNA: n translaation ja estää viruksen lisääntymisen.
Antiviraalinen vaikutus ei ole suunnattu tiettyjä viruksia vastaan (IFN: t eivät ole virusspesifisiä)
· Vuorovaikutus ehjien solujen (infektoimattomien solujen) kanssa estää virusten lisääntymissyklin toteutumisen aktivoimalla soluentsyymejä (proteiinikinaaseja).
· Tämä selittää niiden yleisesti laajan antiviraalisen aktiivisuuden.
Lippu 23
Verenpainelääkkeet
1. KESKUSTOIMEN VALMISTELUT
Analeptikot:
NIKETAMIDI (CORDIAMINE)
SULFOCAMPOCAINE
Adaptogeenit:
GINSENG
LEMONIC Siemen TINCTURE
ELUTEROKOKKAUUTE
2. PERIFERAALINEN TOIMINTA
A. Lisääntynyt OPS, adrenergiset agonistit:
EPINEPHRINE (ADRENALINE)
NOREPINEPHRINE (NORADRENALINE)
fenyyliefriini (MEZATONE)
midodriini (GUTRON)
Kardiotoniset lääkkeet:
1) Adrenomimeetit:
EPINEPHRINE (ADRENALINE) (alfa-beeta-mimeettinen)
DOPAMIINI (beeta-1-mimeettinen)
DOBUTAMIINI (beeta-1-mimeettinen)
2) Sydämen glykosidit:
STROFANTINE
KORGLIKON
B.BCC: n palauttavat varat
1) Lisämunuaiskuoren hormonien valmisteet:
FLUDROCORTISONE
HYDROCORTISON
KORTISONI
2) Veren korvikkeet:
DONORIN VERI
DONOR PLASMA
DEXTRANS: REOPOLYGLUKIN,
GLUKOOSILiuos 5%
Adaptogeenejä (eleutherococcus -uute, sitruunaruoho -tinktuura) suositellaan määrättäväksi yhdessä valerianjuuren tinktuurin kanssa. Eleutherococcuksen ja pantokriinin yhdistelmän tehokkuus todettiin. Jos päänsärkyä esiintyy potilailla, joilla on valtimo hypotensio, kipulääkkeet ovat tehottomia, kun taas kofeiinia ja vaakasuorassa asennossa kivut vähenevät tai häviävät.
1) Kofeiini - ahdistus, levottomuus, unettomuus, takykardia, rytmihäiriöt, kohonnut verenpaine, pahoinvointi, oksentelu. Pitkäaikainen käyttö aiheuttaa lievää riippuvuutta.
2) Adrenaliini - CVS: stä: harvemmin - angina pectoris, bradykardia tai takykardia, sydämentykytys, verenpaineen nousu tai lasku
Sivusta hermosto: useammin - päänsärky, ahdistus, vapina.
Sivusta Ruoansulatuselimistö: useammin - pahoinvointi, oksentelu.
Virtsajärjestelmästä: harvoin - vaikea ja kivulias virtsaaminen (eturauhasen liikakasvua).
Paikalliset reaktiot: kipu tai polttaminen i / m -pistoskohdassa. Allergiset reaktiot: angioedeema, bronkospasmi
3) Norepinefriini - Iskeemiset häiriöt (johtuvat verisuonten supistumisesta ja kudoksen hypoksiasta), refleksibradykardia verenpaineen laskuun, rytmihäiriöt, ahdistuneisuus, ohimenevä päänsärky, hengitysvaikeudet, nekroosi ihon alle.
4) Dobutamiinitahykardia (mukaan lukien kammio), eteisvärinä, sydämen ja rinnan kipu, sydämentykytys, hengenahdistus, kohonnut verenpaine / hypotensio, bronkospasmi.
5) Strofantiini - rytmihäiriöt, dyspeptiset oireet (pahoinvointi, oksentelu), suolilukkoinfarkti, keskushermoston häiriöt
6) Lisämunuaisen kuoren hormonit - Vieroitusoireyhtymä
Omien rauhasten hypotrofian tai atrofian seurauksena (ei-toimivina), koska
hormonia ruiskutetaan liikaa ulkopuolelta), kehittyy akuutti lisämunuaisen vajaatoiminta
jopa sokkiin ja pahennettuihin sairauksiin, joita varten lääke otettiin.
"Steroididiabetes"
Koska se vaikuttaa hiilihydraattien ja rasvojen aineenvaihduntaan.
Cushingin oireyhtymä
Raajojen rasvavarastojen ehtyminen ja rasvan kertyminen kasvoille, kaulalle, hartioille, rintaan.
Heikentynyt immuniteetti
Tuloksena, piilotetut infektiot
Osteoporoosi
Kehittyy pitkäaikaisella hoidolla, voi johtaa patologisiin murtumiin
Natriumin ja veden kertyminen, kaliumin menetys, hypokloreeminen alkaloosi, kohonnut BCC, verenpaine, turvotus
Muut - harvinaisempia - vaikutuksia
Henkinen yliaktiivisuus, ihon ja ihonalaisen kudoksen surkastuminen lisääntyivät
silmänpaine, myopatia, kasvun hidastuminen lapsilla
Keinot hoitoon mahahaava vatsa ja pohjukaissuoli... Luokitus. Gastroprotektiiviset lääkkeet. Toimintamekanismi. Sovellus. Helicobacter pylorin hävittämiseen käytetyt keinot.
TARKOITETTU TERAPIA
1. Keinot, jotka estävät ja poistavat happo-peptisen aggression. (Eli katso edellinen kysymys !!)
2. Keinot, jotka lisäävät limakalvon suojaavia ominaisuuksia.
3. Antihelicobacter.
Decolonization (hävittäminen) apuvälineet Helicobacter pylori
mahalaukun ja pohjukaissuolen limakalvossa.
ANTIHELICOBACTER -LÄÄKEVALMISTEET
(Keinot hävittämiseksi Helicobacter pylori)
Helicobacter pylori
Spiraaliset gramnegatiiviset bakteerit antraalisen limakalvon pinnalla
kalvot solujen välisten liitosten ja rauhasten kaula -alueen sisäisen limakerroksen alla.
Mikrobi voi erittyä mukinaasi, kun taas lima muuttuu vähemmän viskoosiseksi, se menettää suojaavat ominaisuudet.
Tuottaa myös entsyymiä ureaasi, urean jakaminen, mikä johtaa tulokseen
ammoniakkipilvi suojaa mikrobeja suolahapon bakterisidiseltä vaikutukselta.
Mikro -organismi
Aiheuttaa kroonista tulehduksellista gastriittia
Vahvistaa mahalaukun eritysvastetta, mikä johtaa mahahaavan muodostumiseen.
Yleiset säännöt Helicobacter pylorin täydelliseen hävittämiseen:
1. Mikrobilääkkeet tarvitsevat yhdistettyä käyttöä
Se tarjoaa
Tehokkuuden lisääminen vaikuttamalla kehon erilaisiin molekyylikohteisiin
taudinaiheuttaja
Patogeeniresistenssin vähentäminen jollekin lääkkeelle Jos hoito perustuu vismuttipitoisiin lääkkeisiin, lisää
metronidatsoli ja amoksisilliini, tetrasykliini.
3. Antibioottien antimikrobinen vaikutus tehostaa happojen tuotantoa (erityisesti protonipumpun estäjät).
Metronidatsoli Bakterisidinen.
Tehokas antimikrobinen ja antiprotoosinen tarkoittaa.
Toimintamekanismi johtuen nitroryhmän suuresta hapettumisreaktiivisuudesta.
Lääke on "aihiolääke".
Antimikrobista vaikutusta aiheuttaa sen metaboliitti, joka muodostuu mikro-organismissa lääkkeen nitroryhmän palauttamisen seurauksena ferredoksiinin ferruginous-rikki-kompleksin vaikutuksesta. (flavoproteiinien analogi bakteeri- ja alkueläinsoluissa).
Vähentynyt metaboliitti on vuorovaikutuksessa mikrobisolun eri makromolekyylien kanssa, mukaan lukien DNA, proteiinit, kalvon fosfolipidit, mikä aiheuttaa bakterisidisen vaikutuksen.
Yhdistelmä amoksisilliinin kanssa vähentää riskiä metronidatsoliresistenssin kehittymiselle.
Metronidatsolilla on herkistävä vaikutus etanoliin, aiheuttaen jotain alkoholipitoista antabuse -reaktiota (pahoinvointia, oksentelua, päänsärkyä), joten sinun on pidättäydyttävä ottamasta sitä Alkoholijuomat kun käytät metronidatsolia.
Amoksisilliini Puolisynteettinen penisilliini aminopenisilliiniperhe.
Ominaisuudet happokestävyys, bakterisidinen vaikutus, herkkyys penisillinaasille.
Häiritsee bakteerisoluseinän synteesin.
Lääke sitoutuu tiettyyn reseptoriin (penisilliiniä sitova proteiini),
seurauksena on transpeptidaatioprosessin (entsyymitranspeptidaasi) ja proteoglykaanisynteesin rikkominen.
Tämän seurauksena soluseinän autolyyttiset entsyymit (hydrolaasit) aktivoituvat, mikä johtaa sen vaurioitumiseen ja bakteerien kuolemaan. Eli on bakterisidinen vaikutus.
Klaritromysiini Semisynteettinen antibiootti makrolidi(erytromysiiniryhmä)
Sillä on bakteriostaattinen ja bakterisidinen vaikutus.
Häiritsee bakteerien proteiinisynteesiä vuorovaikutuksessa ribosomien 50S-alayksikön kanssa.
Tetrasykliini Klooramfenikoliryhmän antibiootti.
Sillä on bakteriostaattinen vaikutus proteiinisynteesin rikkomisen vuoksi.
Lääke sitoutuu ribosomien 30S-alayksikön reseptoriin.
Kolloidiset vismuttivalmisteet
Hallussapito antibakteerinen vaikutus, mikä häiritsee bakteerien kykyä sitoutua epiteeliin. Niillä on "kalvon muodostava" suojaava vaikutus.
Lisää suojaavan liman ja bikarbonaatin eritystä ja vähentää pepsiinin aktiivisuutta.
Yhdistetyt lääkkeet
Pyloridi (ranitidiini + vismuttisitraatti)
Helicocin (amoksisilliini + metronidatsoli)
Pilobact (klaritromysiini + omepratsoli + tinidatsoli)
Antisekretoiva komponentti:
Omepratsoli (0,02) tai
Lanzopratsoli (0,03) tai
Pantopratsoli (0,04) tai
Rabepratsoli (0,01) tai
Esomepratsoli (0,02)
2 kertaa päivässä
Antimikrobinen komponentti:
Ensilinjan hoito: kolmoishoito
Antisekretoiva komponentti:
Ranitidiinivismuttisitraatti (0,4x2)
Antimikrobinen komponentti:
Klaritromysiini (0,5x2) + amoksisilliini (1,0x2) tai
Klaritromysiini (0,5x2) + metronidatsoli (0,5x2)
Toisen linjan hoito: neliterapia (jos ensimmäinen kurssi on tehoton)
Antisekretoiva komponentti:
Inhibiittori "protonipumppu" vakioannoksena 2 kertaa päivässä
Antimikrobinen komponentti:
Vismuttisubsalisylaatti / -sitraatti (0,120x4) + metronidatsoli (0,5x3) + tetrasykliini (0,5x4)
Esimerkki kaaviosta: 7 päivää
Antisekretoiva komponentti Antimikrobinen komponentti
1) omepratsoli 0,02 2 kertaa päivässä Flemoxin solutab (amoksisilliini) 1,0 2 kertaa päivässä
Fromilid 0,5 2 kertaa päivässä
2) Ranitidiini Klaritromysiini (0,5x2) + amoksisilliini (1,0x2) tai
vismuttisitraatti (0,4x2) klaritromysiini (0,5x2) + metronidatsoli (0,5x2)
GASTROTOKSISUUS VAROITUS
Ei-steroidiset tulehduskipulääkkeet (NSAID)
Paikallisten annostusmuotojen käyttö
Yhdistelmä misoprostolin kanssa
Yhdistelmä erityksen kanssa (protonipumpun estäjät)
Selektiivisten COX 2: n estäjien (meloksikaami, selekoksibi) määrääminen
PVA: ta käytetään virusten aiheuttamien sairauksien ehkäisyyn ja hoitoon.
V. ovat valtavan määrän sairauksien aiheuttajia massiivisista harvinaisiin, eksoottisiin (influenssa, ARVI, tuhkarokko, herpes, hepatiitti, vihurirokko, isorokko, sikotauti, poliomyeliitti, AIDS ...).
V. ovat nukleoproteiinihiukkasia, jotka koostuvat DNA -molekyylistä tai RNA + -proteiinista. Tarttuva osa on DNA, RNA. Se tunkeutuu soluun (eksosytoosin mekanismin avulla) ja siellä alkaa rakentaa uudelleen isäntäsolun aineenvaihduntaprosesseja.
Antiviraalisten aineiden vaikutusmekanismit määräytyvät virusinfektion kehitysvaiheiden mukaan.
Infektion "portit" ovat limakalvot ja iho, tai virus pääsee suoraan verenkiertoon (oksoliinivoide).
Virus pääsee verenkiertoon, leviää kehon läpi → kohdekudos. Voit vaikuttaa virukseen, joka kiertää vapaasti veressä (interferonit ja virusvastaiset vasta -aineet = immunoglobuliinit)
Viruksen tunkeutumisvaihe kohdesoluihin. Virus ei tunkeudu minnekään, vaan sitoutuu vain tiettyyn kalvosolun kohtaan - glykoproteiineilla, jotka ovat viruksen kantajia. Voit: a) estää viruksen kiinnittymisen (tarttumisen) solukalvoon ja estää sen tunkeutumisen isäntäsoluihin; b) virusgenomin (remantadiini) proteiinipitoisuuden estäminen
viruksen lisääntymisvaihe solussa sen jälkeen, kun isäntäsolu on otettu synteettisiin prosesseihin ja luotu oma DNA ja RNA. Jotkut isäntäsoluun tulevat virukset (herpes simplex) alkavat tuottaa omia entsyymejään, jotka eroavat isäntäsolun entsyymeistä (DNA - polymeraasi).
Virusten lisääntymisen estäminen:
virusproteiinien synteesin estäminen: a) "varhaiset" proteiinit - entsyymit, b) "myöhäiset" proteiinit.
Viruksen DNA: n ja RNA: n synteesin estäminen.
Useimmat lääkkeet toimivat näin (viratsoli, asykloviiri ...)
Viruksella tartunnan saaneiden solujen tuhoaminen uusien virusten (interferonien) muodostumisen estämiseksi.
Että. estämään V.I. on välttämätöntä estää virusten tunkeutuminen kohdesoluihin (1, 2, 3) ja hoitoon - häiritä virusproteiinien ja nukleiinihappojen synteesimekanismeja (4) + (5).
Virusinfektiot kehittyvät pääsääntöisesti heikentyneen immuniteetin taustalla. Siksi V.I. - antiviraalisen immuniteetin lisääminen:
A) Erityinen immuunisuoja - rokotteet, immunoglobuliinit (AT), interferonit.
Virusproteiinit ovat sinisiä AG: itä. Viruksille altistuneessa kehossa tuotetaan INF- ja AT -yhdisteitä, jotka neutraloivat virusten toiminnan.
B) Epäspesifinen immuunipuolustus - lisääntynyt vastustuskyky tarttuvat taudit yleisesti. Immunomodulaattorit, IFN -induktorit, vitamiinit, adaptogeenit ...
I. Herpetiset lääkkeet.
Laajin viruslääkkeiden ryhmä. Herpis -virukset voidaan jakaa ryhmiin ottaen huomioon aiheuttamat sairaudet:
A) B. herpes simplex : HSV -1 - iho, limakalvot, HSV -2 - sukupuolielimet, silmät, keskushermosto.
B) V. Garicella Zoster - herpes zoster (aikuiset), vesirokko (lapset), vyöruusu.
V) Sytomegalovirus - verkkokalvontulehdus, paksusuolitulehdus, keuhkokuume, kohdunsisäiset infektiot, yleistyneet infektiot, elinsiirron jälkeiset infektiot jne.
Ihmisen herpesviruksia on vain 8 tyyppiä, sairauksien klinikka on monipuolinen, jopa tappavaan muotoon asti.
Yli 90% maailman väestöstä on tarttunut johonkin herpesvirukseen. Venäjän federaatiossa yli 15 miljoonaa ihmistä sairastuu säännöllisesti HSV: hen.
Se tarttuu ilmassa olevien pisaroiden ja kosketuksen kautta.
Hoito on paikallinen. Jos he sairastuvat useammin kuin 4 kertaa vuodessa - suun kautta, immuniteetilla, systeemisesti. Herpeettisiä infektioita ei voida parantaa. Ensimmäisen tartunnan jälkeen virus pysyy elimistössä koko elämän ajan ja säilyttää kykynsä aktivoitua uudelleen.
HERPES- käännöksessä "hiipivä", joten 2300 vuotta sitten Hippokrates nimitti taudin.
Yksinkertainen : ensimmäiset infektiot lapsuudessa. Tartunta 1–4 -vuotiaana fyysisen kosketuksen kautta aikuisten kanssa. Kahden tunnin kuluttua kosketuksesta virus tunkeutuu ihoon ja saavuttaa kolmoishermon oksat, mikä häiritsee kasvojen ihoa. Sen jälkeen, kun se on tunkeutunut hermokudokseen, se tunkeutuu kallon onteloon ja pysyy eliniän kolmoishermoissa. Siellä hän on "lepotilassa" uudelleenaktivointihetkeen asti (vilustuminen, flunssa, kuukautiset, stressi, väsymys, voimakas UV -säteily ja muut olosuhteet ↓ immuniteetti ..).
Huulilta voi mennä muihin kehon osiin (silmät, suuseksi, ... otsa, posket, korvat ...).
Virus ei pidä UV, alkoholi, antiseptiset aineet ...
Keskushermoston herpes - vakavin keskushermoston infektio. Kuolleisuus 70%, toimintojen palautuminen 9%.
Herpes zoster - vesirokkoa sairastaneet aikuiset sairastuvat. Ihottuma kehon toisella puolella, monet nesteellä täytetyt rakkulat, erittäin tuskallista, useita viikkoja + päänsärkyä, tº, kipu jaloissa, selkärangassa ... Ihottumien katoamisen jälkeen herpeettinen neuralgia on 20-30% ja on huonosti hoidettu.
Nukleidien analogit.
Nukleosidien synteettisillä johdannaisilla on voimakas selektiivinen antiherpeettinen vaikutus.
Vaikutusmekanismi: aineilla ei ole antiherpeettistä vaikutusta, vaan niiden aktiivisilla metaboliiteilla - trifosfaateilla. Viruksessa tartunnan saaneessa solussa kolme fosfaattimolekyyliä on kiinnittynyt lääkkeeseen. Tuloksena oleva aine estää viruksen DNA -polymeraasia, integroituu virus -DNA: han (deoksiguanosiinin tai muun aineen sijasta) ja estää sen replikaatiota (eli DNA -ketjun jatkaminen jatkuu, koska trifosfaattiaineella ei ole kiinnittymiseen tarvittavaa tilaa) seuraavista DNA -linkeistä).
ZF = L - F - F - F
Terveissä soluissa keskittyminen
trifosfaatti 50-100 kertaa pienempi kuin
viruksen aiheuttamat solut, koska
ensimmäisen fosfaatin lisääminen
jonka suorittaa entsyymi
esiintyy vain herpesviruksessa = virus
tymiinikinaasi.
Toisen ja kolmannen fosfaatin kiinnittymisen suorittavat solun entsyymit = kinaasit, eivät virus. Nuo. terapeuttinen annos ei toimi terveessä solussa, vain sairaassa.
Tällaiset lääkkeet ovat tehokkaimpia taudin alkuvaiheessa (1-3 päivää), koska vaikuttaa aktiivisesti lisääntyviin viruksiin. Toiminta on ennaltaehkäisevää ja parantavaa.
ACYCLOVIR(zorirax, virolex, tsilovir ...) on guanosiinijohdannainen.
Vaikuttava aine on asykloviiritrifosfaatti, joka on upotettu viruksen DNA: han deoksiguanosiinin sijaan.
F. -. suun kautta otettava biologinen hyötyosuus on alhainen, 15-20%, mutta se on hyvin jakautunut: se tunkeutuu sylkeen, silmänsisäiseen nesteeseen, emättimen eritteisiin, keskushermostoon ja herpeettisten rakkuloiden nesteeseen. Imeytyy hieman paikallisesti.
Spektri: suurin aktiivisuus HSV_1.2: ta vastaan, heikompi VG: lle, Zosterille ja epäherkkä sytomegaviruksille.
PC: a) HSV: n aiheuttamat infektiot - iho, limakalvot, silmät, sukupuolielinten herpeettinen aivotulehdus
b) vyöruusu, vesirokko
c) ennaltaehkäiseviin tarkoituksiin potilailla, joilla on ID (toistuvat muodot)
F.V. kerma 5%, silmävoide 3%, pöytä, 0,02, 0,04, 0,08, kapselit 0,02, ampullit jauheella liuoksen valmistamiseksi (0,25, 0,5, 1,0). Kurssit 7-10 päivää × 5 r / d.
PBD: alhainen myrkyllisyys.
Paikallisesti - polttaminen, kutina, laskimotulehdus.
Systeeminen - ruoansulatuskanava, IV - munuaistoksisuus, neurotoksisuus (kouristukset, letargia, ekstrapyramidaaliset häiriöt, päänsärky jne.)
Asykloviiri tulee määrätä mahdollisimman aikaisin, myöhemmässä vaiheessa se on lähes passiivinen.
VALANCYCLOVIR(valtrex) - asykloviirivaliiniesteri. Suun kautta annettavaksi. Sillä on korkea hyötyosuus, yli 50% (eetteri puristuu pois kehosta, eli asykloviirin terapeuttinen pitoisuus kudoksissa).
PC: HSV -infektiot - erityisesti sukupuolielimet, vyöruusu jne.
F.V. välilehti. 0,5 × 2 r / d. kurssi on 7-10 päivää.
PENCYCLOVIR(Vectavar) - rakenteeltaan aktiivisuus on lähellä asykloviiria.
Erot :
Aktiivinen joitakin asykloviirille resistenttejä viruskantoja vastaan
Tehokkaampi H: n myöhemmissä vaiheissa
Pidempi T1 / 2 solun sisällä (7-20 tuntia), ts. toimii 12 tuntia
Käytä vain paikallisesti
PC: ihon ja limakalvojen herpes.
F. sisään... kerma 1% × 2r / d kurssi 4 päivän ajan.
FANCYCLOVIR(famvir) - hyötyosuus 70-80%. Elimistössä (veri, suolet, maksa) se muuttuu pentsikloviiriksi → P-trifosfaatiksi, erittyy munuaisten kautta 70% aktiivisessa muodossa.
Spektri: erilaiset herpesvirukset.
PC: toistuva sukupuolielinten herpes, vyöruusu, postherpeettinen neuralgia.
F. sisään... välilehti. 0,25.
PBD: dyspepsia, neurotoksisuus.
GANCYCLOVIR
Spektri: vaikuttaa sytomegalovirukseen. 10-15 kertaa vahvempi kuin hemasykloviiri.
F. -. imeytyy huonosti ruoansulatuskanavasta, mutta jakautuu hyvin eri kudoksiin. Se erittyy munuaisten kautta.
PC: verkkokalvontulehdus, keuhkokuume, ruoansulatuskanavan vauriot, IMV - β - infektiot AIDS -potilailla.
PBD: usein ≈ 1/3 potilaista aiheuttaa peruutuksen (maksatoksisuus, CVS, munuaistoksisuus, neurotoksisuus, ruoansulatuskanava, laskimotulehdus).
F. sisään... 0,25 kapselia, injektiopullo, injektiokuiva -aine.
IDOXUREDIN(oftan-IDU) on rakenteeltaan tymidiinin analogi.
PC: korkea aktiivisuus paikallisten herpeettisten vaurioiden hoidossa (keratiitti, sidekalvotulehdus)
F. sisään... silmätipat 0,1% liuos, tiputettu 2 tunnin välein.
PBD: ärsytys, kipu, limakalvojen turvotus.
Resorptiivisella toiminnalla (IV) se on tehokas yleistyneelle herpesille. Mutta erittäin korkea toksisuus (↓ leukopoieesi)
YRITYSTUOTTEET
ALPIZARIN- kasviperäinen aine (penniin yrtistä, mangolehdistä). Kemiallinen rakenne on ksanonijohdannainen (P -vitamiinin analogi).
Estää DNA-pitoisuuden lisääntymistä
viruksia. Sisältää virus-,
bakteeri, immunomoduloiva
Tietoja toiminnasta.
F.w.: Välilehti. 0,1, voide 5% - iho, 2% - limakalvot.
PC: ihon ja limakalvojen herpes simplex, Zosterin herpes (yksinkertainen, sukuelinten 2, vesirokko, vyöruusu, syyliä, kandidiaasi).
Sisällä x 3-4 r / d-5-10 päivää. samanaikaisesti
Voide x 3-3 r / d-10-30 päivää
Voit käyttää pillereitä ennaltaehkäiseviin tarkoituksiin.
GLYKYYRIHAPPO
Vaikutusmekanismi: a) ↓ sisäisten proteiinien ja muiden komponenttien synteesi tartunnan saaneessa solussa, b) inaktivoi virukset solun ulkopuolella, c) estää viruksen pääsyn soluun.
PC: yksinkertaisen hepatiitin 1 ja 2 viruksen aiheuttamat infektiot (iho, suun limakalvot, nenä ... sukupuolielinten herpes), herpes zoster jne.
PBD: allergiset reaktiot
F.w .: spray, kerma, emätinmuodot.
FLAKOSIDI- sametin (Amur, Laval) kasvin lehdistä tämä. Rutovs.
Rakenne on samanlainen kuin alpitsariini.
PC: primaarinen tai toistuva herpes simplex (alkuvaiheet).
F.w.: Välilehti. 0,1 x 3 r / d, kurssi 5 päivää. ja enemmän.
Herpesinfektioiden monimutkaisessa hoidossa roncoleukiinia (rekombinantti interleukiini-2) voidaan käyttää eri muodoissa ja taudin eri vaiheissa.
II. FLU- JA ARVI -KÄSITTELYTAVAT.
AMANTADINE- ensimmäinen lääke, jolla on todistettu viruslääke
RMANTADINE toiminta. Nykyään tätä tietokonetta ei käytetä.
Sen perusteella rimantadiini on kehitetty Venäjän federaatiossa.
Toimintamekanismi: estää viruksen erityiset ionikanavat (M 2 -kanavat), minkä seurauksena sen kyky tunkeutua soluun häiriintyy. M2 -kanava on proteiini, jota esiintyy vain influenssaviruksessa ja joka on vastuussa viruksen genomin vapautumisesta soluun (M 2 - tuottaa viruksen "riisumista" = deprotoinisaatio).
FC: imeytyy hyvin ja jakautuu suun kautta, tunkeutuu keskushermostoon, suuret pitoisuudet nenän ja syljen limakalvolla; maksa; munuaiset.
Spektri: influenssa A -virusta (on resistenttejä kantoja).
PC: a) ehkäisy 0,5 x1 r / d tai 0,1 x2 r / d - kurssi on 14 päivää.
b) hoito alkuvaiheessa 0,1 x 2 r / vrk tai järjestelmän mukaisesti
PBD: dyspepsia, vatsakipu, keskushermosto, ihottuma.
PPK: maksa, munuaiset, tyreotoksikoosi, raskaus.
FV: välilehti. 0,05 "Algirem" - siirappi lapsille.
Riippuvuus syntyy nopeasti (5 päivässä jopa 30%).
Sikainfluenssa = pandemia. Remantadine ei toimi.
OZELTAMIVIR- korkea spesifisyys, ei muille viruksille
ZANAMIVIR toimia. Se on määrätty ensimmäisten 24-48 tunnin aikana oireiden alkamisesta.
Ne ovat rakenteeltaan ja toimintamekanismiltaan samanlaisia.
Toimintamekanismi: estävät neuromedase -aktiivisen kohdan - entsyymin, joka on vastuussa uusien muodostuneiden viruspartikkeleiden vapautumisesta tartunnan saaneista soluista, niiden tunkeutumisesta hengitysteiden epiteelisoluihin ja viruksen leviämisestä kehossa.
PC: tyypin A ja B + influenssapandemia.
ZANAMIVIR - hoito. F.V .: hengitettynä- rotodiskit, jotka sisältävät 0,005 kerta -annosta. Hengitys, koska imeytyy huonosti ruoansulatuskanavasta (jauhe hengitetään). Paikallisesti käytettäessä PBE on harvinainen (dyspepsia, päänsärky, bronkospasmi - alttius). Määritä 5 vuodesta alkaen 2 r / d, kurssi 5 päivää. Ei vastusta.
OZELTAMIVIR (lääke) - imeytyy hyvin, hyötyosuus 75-80%. Korkeat pitoisuudet influenssa -infektion keskipisteissä. Lapset 1 -vuotiaasta alkaen.
PBD: dyspepsia, päänsärky, heikkous, unihäiriöt (useammin kuin tsanamiviirilla), kurkkukipu, yskä.
F.V. kapselit 0,075.
Influenssan hoito ja ehkäisy. Osittainen vastustuskyky influenssapandemiaa vastaan.
ARBIDOL- indokin johdannainen. Sillä on kohtalainen antiviraalinen vaikutus, interferonien indusoija, immunomoduloiva vaikutus; lisää kehon vastustuskykyä virusinfektioille.
PC: influenssa A: n ja B: n epäspesifinen ehkäisy ja hoito, ARVI.
F.V. välilehti. 0,1, hoito x 3-4 r / d 3-5 päivää, ennaltaehkäisy x 1 r / d 10-14 päivää.
PBD: allergia.
PPc: CVS, maksa, munuaiset.
OXOLIN- naftaleenijohdannainen, vanha lääke.
Toimintamekanismi: ≈ kuten remantadiinissa (solunulkoinen virus).
Kohtalainen virisidinen vaikutus.
PC: 1) influenssan ehkäisy
virusten silmävauriot
3) virus nuha
4) ihon projektio
F. sisään... oksaali voide - 0,25%, 3%
Flunssa, voitele nenän limakalvo x 2-3 r / d
PBD: palaa käyttöpaikalla.
Influenssan hoitoon ja ehkäisyyn voidaan käyttää seuraavia:
Interferoni alfa-2v(influenssa) (yhdistelmälääke) - nenätipat. Viferon
INF -induktorit: " Anaferon"- homeopatia
Cieloferon
Kagocel
Arbidol
Antiviraaliset aineet ovat eri kemiallisten rakenteiden aineita, jotka estävät virusten pääsyn soluihin, syntetisoivat viruksen nukleiinihappoja ja proteiineja sekä replikoivat viruksia.
V viime vuodet virusten aiheuttamien sairauksien esiintyvyys on lisääntynyt. Tunnetaan noin 500 ihmiselle patogeenistä virustyyppiä. On osoitettu, että virustartunta aktivoi useita biokemiallisia prosesseja isännän kehossa. Antiviraalisten aineiden toiminnan tarkoituksena on estää nämä prosessit.
Antiviraalisille aineille on ominaista seuraavat toimintamekanismit
1. Viruksen adsorption ja sen tunkeutumisen isäntäsoluun rikkominen ( γ-pallot).
2. Viruksen genomin vapautumisen rikkominen ( midantan , remantadiini).
3. Nukleiinihappojen synteesin rikkominen ( tsidovudiini , asykloviiri , vidarabiini).
4. Virusproteiinien synteesin rikkominen:
Virionien rakentaminen ("keräävät" virionit) ( metisazon)
- "myöhäiset" virusproteiinit ( sakinaviiri).
5. Lääkkeet, joilla on laaja vaikutusalue (interferonit: laferon , referoni , beetaferoni jne.).
Nykyään lääketiede käyttää noin 30 viruslääkettä. Kaikki interferoneja lukuun ottamatta ovat synteettisiä huumeita.
Seuraavat viruslääkeryhmät ovat käytännössä tärkeitä:
1) influenssalääkkeet;
2) antiherpeettiset ja antimegaloviruslääkkeet;
3) ihmisen immuunikatovirukseen vaikuttavat aineet;
4) varat, jotka vaikuttavat retroviruksiin ja pikornaviruksiin;
5) variola -virukseen vaikuttavat aineet;
6) laajakirjoiset lääkkeet (mukaan lukien hepatiitti B ja C).
Influenssalääkkeet
Luokitus:
1. Lääkkeet, jotka estävät virusproteiini M2: remantadiini , midantan (amantadiini).
2. Lääkkeet, jotka estävät virusentsyymin neuraminaasia: tsanamiviiri , oseltamiviiri .
3. Lääkkeet, jotka estävät viruksen RNA -polymeraasia: ribaviriini .
4. Erilaiset lääkkeet: arbidol , oksoliini , interferonit .
Proteiini M2 on influenssaviruksen spesifinen proteiini. Se sisältyy viruksen kalvoon ja toimii ionikanavana. Tämän proteiinin salpaajat häiritsevät viruksen "riisumista" ja estävät viruksen genomin vapautumisen isäntäsolussa. Tämän seurauksena viruksen replikointiprosessi on häiriintynyt.
Midantan käytetään kuitenkin tyypin A viruksen ehkäisyyn, mutta lääkkeellä on kuitenkin alhainen tehokkuus, mikä rajoittaa sen käyttöä tähän tarkoitukseen. Pääasiassa midantaania käytetään parkinsonismin hoitoon. Lääke imeytyy helposti maha -suolikanavasta, erittyy virtsaan. Tehokkaampi influenssaa vastaan on remantadiini .
Remantadiini . Farmakokinetiikka. Lääke imeytyy helposti maha -suolikanavasta, 10 % metaboloituu maksassa, erittyy munuaisten kautta (90 % erittyy muuttumattomana erittymisen kautta). Yleensä potilaat sietävät lääkettä hyvin.
Farmakodynamiikka. Lääke estää influenssaviruksen RNA: n vapautumisen ja tunkeutumisen solun ytimeen. Lisäksi se estää viruksen DNA-riippuvaisen RNA-polymeraasin induktion, vähentää viruksen RNA: n ja proteiinin synteesiä. Lisäksi lääke estää neuraminidaasin ja estää tartunnan saaneisiin soluihin liittyvän viruksen leviämisen. Viruksen replikaatio on myös häiriintynyt. Neuraminidaasi on influenssa A- ja B -virusten pinnalla sijaitseva glykoproteiini, joka helpottaa viruksen tunkeutumista hengitysteiden kohdesoluihin.
Käyttöaiheet. Remantadiini on tehokas virusta A (erityisesti A2) vastaan. Lääke vaikuttaa myös punkki-enkefaliittivirukseen. Influenssan ehkäisemiseksi remantadiinia määrätään suun kautta 0,05 g. Lääkkeen oikea -aikainen käyttö 50% tai enemmän vähentää influenssan esiintyvyyttä epidemioiden aikana, ja sairauden tapauksessa infektio kulkee lievässä muodossa. Lääkkeen ottaminen 2-3 päivää taudin puhkeamisen jälkeen on tehotonta, ja 5 päivän kuluttua se on täysin hyödytöntä. Punkki-enkefaliitin ehkäisemiseksi remantadiinia määrätään 0,1 g (2 tablettia) kahdesti päivässä 3-5 päivän ajan (ehkäisy alkaa heti punkin puremisen jälkeen).
Sivuvaikutukset. Haittavaikutuksia ovat dyspepsia, ärtyneisyys, päänsärky, unettomuus, huimaus. Remantadiini on vasta -aiheinen raskaana oleville naisille, koska lääkkeellä on teratogeenisia ja sikiötoksisia vaikutuksia.
Oseltamiviiri ja tsanamiviiri ovat aihiolääkkeitä. Imeytymisen jälkeen ne muuttuvat aktiiviseksi muotoksi.
Zanamivir (Relenza) käytetään intranasaalisesti tai inhalaationa jauheen muodossa. Tässä tapauksessa noin 15% annetusta annoksesta pääsee systeemiseen verenkiertoon. Lääke erittyy munuaisten kautta.
Oseltamiviiri (Tamiflu) nimetä sisälle.
Farmakokinetiikka. Lääke imeytyy helposti ruoansulatuskanavasta, käy läpi nopean hydrolyysin suolistossa, maksassa ja veressä. Sen aktiivisten metaboliittien hyötyosuus on noin 80%. Lääke erittyy munuaisten kautta.
Farmakodynamiikka. Vaikutusmekanismi on influenssa A- ja B -virusten neuraminidaasin estäminen, niiden aggregaation rikkominen, poistuminen solusta. Lääkkeet vähentävät flunssan oireiden vakavuutta, lyhentävät kuumekauden kestoa, vähentävät komplikaatioiden esiintyvyyttä ja nopeuttavat viruksen poistumista kehosta.
Käyttöaiheet: influenssan ja siihen liittyvien sairauksien (keuhkoputkentulehdus, keuhkokuume) hoito yhdessä antibioottien kanssa.
Sivuvaikutus pahoinvointi ja oksentelu, ripuli, epigastrinen epämukavuus, kutina, lihaskipu, ossalgia, päänsärky, parestesia, huimaus, vatsakipu, suun limakalvon haavaumat.
Ribaviriini on guanosiinijohdannainen.
Farmakokinetiikka. Se imeytyy hyvin suolistosta, suurin pitoisuus veressä 1-1,5 tunnin kuluttua.Eritetään munuaisten kautta, T, Aseta 24 tuntia, mutta plasmassa pysyy 16 päivää. Lääke fosforyloituu kehossa.
Farmakodynamiikka. Ribaviriinimonofosfaatti, joka muodostuu ribaviriinin fosforylaation seurauksena, estää guaniininukleotidien synteesiä ja trifosfaatti estää viruksen RNA -polymeraasia ja häiritsee mRNA: n muodostumista.
Käyttöaiheet. Ribaviriini on tehokas influenssa A: lle ja B: lle, vakavalle hengityselinten synkytiaaliselle virusinfektiolle, verenvuotokuumeelle ja munuaisten oireyhtymälle. Se vaikuttaa parainfluenssaan, tuhkarokkoon, ihmisen immuunikatoviruksiin, reo-, rabdo-, tonga-, Arena-viruksiin, rokkoviruksiin jne.
Sivuvaikutukset. Kun lääkettä otetaan, ihottumaa, sidekalvotulehdusta voidaan havaita. Ribaviriinilla on mutageenisia, teratogeenisiä ja karsinogeenisia ominaisuuksia.
Influenssan monimutkaisessa hoidossa määrätään interferoni -induktoreita: Amizon, mefenamiinihappo, amiksiini, sykloferoni, groprinosiini, polyoksidonium, proteflatsidi, arbidoli jne. (Katso alla).
Influenssan ehkäisyyn ja hoitoon määrätään virusideja, jotka vaikuttavat virukseen solunulkoisesti ja estävät tunkeutumisen soluun. Näitä ovat oksoliinivoide.
Oxolin tarkoitettu influenssan ehkäisyyn, virusperäisen nuhan, adenoviruskeratokonjunktiviitin, herpeettisen keratiitin, joidenkin virusinfektioiden (vyöruusu jne.) kanssa. Sitä käytetään voiteen muodossa, joka levitetään nenän limakalvolle, asetetaan alemman silmäluomen taakse tai iholle. Haittavaikutuksista johtuen kauterisaation tunne käyttöpaikalla on mahdollinen.
Mitä muuta luettavaa
VIIMEISET HUOMAUTUKSET
- Kuinka miellyttää rakastettua miestäsi, poikaystävääsi tai ystävääsi: epätavallisia yllätyksiä Mitä tehdä tehdäksesi vaikutuksen kaveriin
- Koiranpaskaa kotona: miten vieroittaa?
- Uusia aforismeja
- Kuinka ottaa aurinkoa auringossa - nopea ja oikea rusketus
- Plutarch - elämäkerta, tiedot, henkilökohtainen elämä Plutarch elämänvuosia